Радиосенсибилизатор
Cтраница 1
Радиосенсибилизаторы усиливают, а радиозащитные факторы ( в частности, протекторы) ослабляют действие радиации на организм и отдельные биологические объекты. [1]
Эти результаты подтверждают представление о возможности одновременного применения радиосенсибилизаторов для повышения чувствительности клеток к облучению и радиопротекторов для защиты клеток окружающих здоровых тканей. [2]
Наряду с радиопротекторами интерес радиобиологов вызывают вещества с противоположным действием - радиосенсибилизаторы. Их значение определяется повышением чувствительности клеток опухолевой ткани к облучению. Радиопротекторы и радиосенсибилизаторы вместе представляют так называемые радиомодифицирующие средства. [3]
В последние годы успешно развивается новое направление радиобиологии-поиск и исследование соединений с противоположным радиопротекторам действием - радиосенсибилизаторов. Одной из главных целей здесь является изыскание химических соединений, повышающих чувствительность раковых клеток к воздействию ионизирующей радиации. Таким образом, проблемы защиты здоровых тканей с помощью радиопротекторов и повышение чувствительности раковых клеток к облучению путем использования радиосенсибилизаторов оказываются связанными общностью задач. [4]
С изложенной точки зрения перспективным направлением в создании радиоактивного лекарства является синтез соединения, сочетающего свойства радиосенсибилизатора к излучению включенного изотопа со свойствами группы химических веществ, которые сами по себе оказывают разрушающее действие на клетки опухоли. [5]
Основная задача, которая стоит перед специалистами, занятыми решением проблемы радиоактивной лекарственной терапии опухолей, заключается в синтезе соединений, сочетающих свойства радиосенсибилизаторов со свойствами группы химических веществ, которые сами по себе оказывают разрушительное действие на клетки опухоли. Если же ввести в эти соединения радиоактивные изотопы, которые должны селективно поглощаться в течение некоторого промежутка времени раковыми клетками, то испускаемые входящими в состав соединения радиоактивными атомами излучения будут также разрушать опухоли. [6]
Можно предположить, что заметные количества защитных тиолов, присутствующих в нормальных условиях в тканях ( глютатион, цистеин, гомоцистеин), существуют частично в форме смешанных дисульфидов с молекулами мишени; что радиосенсибилизаторы группы цистеин - цистеамин отделяют молекулы мишени от их защитных остатков из-за большей склонности образовывать смешанные дисульфиды с естественно встречающимися защитными веществами, чем с молекулами мишени. [8]
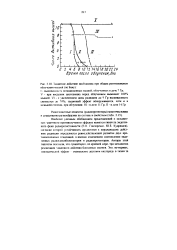 |
Защитное действие цистеамина при общем рентгеновском облучении мышей ( по Баку. [9] |
Наиболее удачным обобщением представлений о механизмах защитного противолучевого эффекта является гипотеза эндогенного фона радиорезистивности ( Е.Н. Гончаренко, Ю.Б. Кудряшов), согласно которой устойчивость организмов к поражающему действию радиации определяется равнодействующей развития двух противоположных тенденций, а именно изменением соотношения эндогенных радиосенсибилизаторов и радиопротекторов. Авторы этой гипотезы показали, что существуют, по крайней мере, три механизма реализации защитного действия биогенных аминов. [10]
Установлено, что перекись метилэтилкетона вызывает снижение уровня сульфгидрильных групп в крови и угнетение активности каталазы, чем логично, по-видимому, объяснить и радиосенсибилизирующее действие этого вещества. Действительно, многочисленные радиосенсибилизаторы из числа галоидсодержащих производных ртути являются веществами, снижающими уровень SH-групп в крови. Исходя из этого положения можно было ожидать, что радиосенсибилизи-рующим действием должны обладать также и альдегиды. Известно, что альдегиды легко вступают в реакцию конденсации с тиолами с образованием полумеркапталей или полумеркаптолей. Последние при взаимодействии со второй молекулой тиола дают полные меркаптали. Следовательно, воздействие альдегидов на организм может сопровождаться снижением уровня сульфгидрильных групп и повышением радиочувствительности животных. Это предположение было проверено нами совместно с П. А. Колесниковым и Л. В. Ивановой ( 1971) в опытах с формальдегидом. [11]
Эффективность радиационного воздействия на опухоль можно повысить, увеличив чувствительность опухолевых клеток к облучению, воздействуя на них химическими агентами - радиосенсибилизаторами опухолевых клеток к облучению. Непременным условием применения химических радиосенснбилизаторов является избирательная сорбция их опухолевыми клетками. [12]
Изменение радиочувствительности тканей организма имеет большое практическое значение. Данная книга посвящена радиопротекторам, а также веществам, снижающим радиочувствительность организма, однако это не означает, что мы недооцениваем исследования радиосенсибилизаторов; их изучение ведется прежде всего в интересах радиотерапии. [13]
Вдовенко, В. Н. Бобровой с сотрудниками первый отечественный препарат 2-метил - 1 4-нафтогидрохинондифосфата натрия прошел лабораторные испытания в Научно-исследовательском институте онкологии им. Научно-исследовательском институте онкологии и медрадиологии МЗ БССР, где была определена его острая и хроническая токсичность и разработана инструкция клинического испытания в качестве радиосенсибилизатора опухолевых тканей к рентгеновскому облучению. [14]
Большое значение в защитном действии гаммафоса придают напряжению кислорода в клетках. Было многократно показано, что защита кожи гаммафосом более выражена, если мыши вдыхают воздух, а не кислород. Радиосенсибилизатор гипоксических клеток мизо-нидазол, вводимый в комбинации с гаммафосом, приводит к снижению его защитного действия в коже и опухолях. Аналогично этому, сенсибилизирующее действие мизони-дазола ослабевает в присутствии гаммафоса. Результаты дают основания предполагать, что оба вещества действуют на одном уровне радиационного поражения. Кроме того, они демонстрируют, что гаммафос проникает в гипокси-ческие клетки опухоли. [15]
Страницы: 1 2
