Кажущийся радиус - атом
Cтраница 1
Кажущийся радиус атома у Со наименьший, а у Rh и Ir они почти равны. [1]
 |
Физические константы простых веществ четвертой подгруппы р-элементов. [2] |
Кажущиеся радиусы атомов в валентном состоянии 4 растут с увеличением порядкового номера атома, в связи с чем их окислительная способность падает; исключение составляет РЬ4, являющийся очень сильным окислителем. [3]
Кажущиеся радиусы атомов последних двух элементов практически одинаковы. [4]
Название кажущиеся радиусы атомов и ионов, вычисляемые по данным кристаллографических измерений, принято потому, что эти величины ни в коем случае не означают действительного протяжения атомов или ионов: они только указывают, до каких пределов центры атомов или ионов могут взаимно сближаться при образовании кристаллических соединений. Эти расстояния являются некоторыми величинами, обусловленными природой соответствующих атомов или ионов, которые хотя и не строго постоянны, но, как показывает опыт, могут - в первом приближении приниматься за постоянные величины. Другими словами, атомы и ионы в соответствии с опытными данными ведут себя в кристаллах практически как твердые ( не изменяющие своих размеров) или почти твердые шары; величину радиусов этих шаров и дают кажущиеся атомные и ионные радиусы. [5]
Название кажущиеся радиусы атомов и ионов, вычисляемые по данным кристаллографических измерений, принято потому, что эти величины ни в коем случае не означают действительного протяжения атомов или ионов: они только указывают, до каких пределов центры атомов или ионов могут взаимно сближаться при образовании кристаллических соединений. Эти расстояния являются некоторыми величинами, обусловленными природой соответствующих атомов или ионов, которые хотя и не строго постоянны, но, как показывает опыт, могут в первом приближении приниматься за постоянные величины. Другими словами, атомы и ионы в соответствии с опытными данными ведут себя в кристаллах практически как твердые ( не изменяющие своих размеров) или почти твердые шары; величину радиусов этих шаров и дают кажущиеся атомные и ионные радиусы. Совершенно такие же величины ионных радиусов, какие получил Гольдшмидт чисто эмпирически на основании измерений межатомных расстояний в кристаллах, рассчитал теоретически Енсен ( 1938) на основании принципов волновой механики. [6]
Название кажущиеся радиусы атомов и ионов, вычисляемые по данным кристаллографических измерений, принято потому, что эти величины ни в коем случае не озна-нают действительного протяжения атомов или ионов: они только указывают, до каких пределов центры атомов или ионов могут взаимно сближаться при образовании кристаллических соединений. Эти расстояния являются некоторыми величинами, обусловленными природой соответствующих атомов или ионов, которые хотя и не строго постоянны, но, как показывает опыт, могут в первом приближении приниматься за постоянные величины. Другими словами, атомы и ионы в соответствии с опытными данными ведут-гсебя в кристаллах практически как твердые ( не изменяющие своих размеров) или почти твердые шары; величину радиусов этих шаров и дают кажущиеся атомные и ионные радиусы. Совершенно такие же величины ионных радиусов, какие получил Гольдшмидт чисто эмпирически на основании измерений межатомных расстояний в кристаллах, рассчитал теоретически Енсен ( 1938) на основании принципов волновой механики. [7]
Если проследить за изменением величин кажущихся радиусов атомов лантаноидов ( рис. 48), то от первого элемента - церия к последнему - лютецию, исключая аномалию у европия и иттербия, они постепенно уменьшаются: это явление получило название лантаноидного сжатия, или контракции. Лантаноидная контракция имеет большое значение для обсуждения свойств элементов, стоящих в VI периоде после 71 элемента. [8]
Ионизационные потенциалы также падают от азота к висмуту с ростом кажущегося радиуса атома. [9]
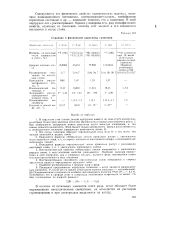 |
Строение и физические константы галогенов. [10] |
Все атомы галогенов образуют отрицательные ионы типа R - и тем Легче, чем меньше кажущийся радиус атома. [11]
Атомы химического элемента не имеют строго Определенных размеров, что обусловлено двойственной природой электронов. Пользуются эффективными или кажущимися радиусами шарообразных атомов, сближенных при образовании кристаллов. [12]
Длина связи или расстояние между атомами определяется в первую очередь размерами атомов, соединенных связью. Для настоящей цели кажущийся радиус может быть принят для отдельного атома таким, чтобы сумма кажущихся радиусов атомов была равна длине связи. На длину связи в некоторой степени также влияет прочность связи: чем прочнее связь, тем короче длина. Поэтому кажущийся атомный радиус будет изменяться с типом связи; например, кажущийся атомный радиус углерода для одинарной ковалентной связи равен 0 77 А, для двойной связи он понижается до 0 67 А и для тройной связи до 0 60 А. [13]
Страницы: 1