Разбавление - азотная кислота
Cтраница 3
Решающее значение в данных условиях имеет также температура, так как ее повышение в зоне осушки газов приводит к увеличению давления насыщенных водяных паров, что в свою очередь вызывает разбавление азотной кислоты и уменьшение содержания в ней окислов азота. [31]
Тепло, расходуемое при концентрировании азотной кислоты с 48 до 98 % HNO3, определяется из следующих данных: теплота ( разбавления азотной кислоты со 100 до 48 % HNOa равна 6300 ккал / моль; теплота разбавления азотной кислоты со 100 до 98 % HNO3 составляет 400 ккал / моль. [32]
Как известно, такого рода реакции идут лишь с разбавленной азотной кислотой н при нагревании, вследствие чего азотная кислота не только нитрует боковую цепь, но в большой степени ее окисляет. Разбавлением азотной кислоты уксусной кислотой можно в значительном степени увеличить выход нитросоединения с нитрогруп-пой в боковой цепи, не прибегая к повышению температуры. [33]
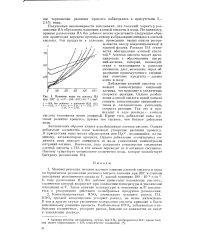 |
Влияние воды на распад НА при 200 и m / F ( 89 - 107 - 10 - 4 г / см3. [34] |
Добавление азотной кислоты повышает концентрацию нитропий-катиона, что приводит к увеличению скорости реакции. Однако разбавление азотной кислоты водой должно снизить концентрацию нитроний-ка-тиопа и, следовательно, уменьшить скорость реакции. [35]
В некоторых опытах М. И. Коновалов применял азотную кислоту и других концентраций; однако с увеличением концентрации азотной кислоты увеличивается количество образующихся полинитросоединений, а также продуктов окисления. С разбавлением азотной кислоты уменьшается образование побочных продуктов реакции, но снижается и нитрующая способность азотной кислоты. [36]
Аналогично ведет себя и метиловый эфир. При разбавлении азотной кислоты водой выход фуроксанового соединения быстро снижается, сводясь к нулю при концентрации 70 - 75 %, так как при разбавлении быстро уменьшается содержание в растворе ионов нитрония. [37]
Аналогично ведет себя и метиловый эфир. При разбавлении азотной кислоты водой выход фуроксанового соединения быстро снижается, сводясь к нулю при концентрации 70 - 75 %, так как при разбавлении быстро уменьшается содержание в растворе иоиов нитрония. [38]
Кроме того, как известно, азотная кислота является окислителем. При разбавлении азотной кислоты ее окислительное действие на ароматическое соединение усиливается. [39]
Животные и растительные ткани при действии на них азотной кислоты подвергаются нитрованию. По мере разбавления азотной кислоты ее окислительные свойства ослабляются, а кислотные усиливаются. Поэтому реакции многих металлов с разбавленной азотной кислотой протекают с вытеснением водорода, который расходуется на дальнейшее восстановление избытка азотной кислоты до смеси различных продуктов ее восстановления. [40]
Замещение атомов водорода в ароматическом ядре на нитро-группу происходит при действии концентрированной азотной кислоты. Во избежание нежелательного разбавления азотной кислоты, выделяющейся при реакции водой, применяют небольшой избыток дымящей азотной кислоть. [41]
С понижением концентрации азотной кислоты при нитровании становится заметным выделение оксидов азота. Чтобы избежать отрицательного влияния на процесс нитрования разбавления азотной кислоты, ее берут в большом избытке. Более эффективным является введение в реакционную массу в качестве водоотнимающего средства концентрированной серной кислоты. [42]
Азотной кислоте, в отличие от ряда других кислот ( соляная, разбавленная серная и др.), присущи не только кислотные, но и окислительные свойства. Концентрированная азотная кислота обладает сильно выраженными окислительными свойствами, при последовательном разбавлении азотной кислоты эти свойства быстро ослабевают и возрастает коэффициент активности, характеризующий ее кислотные свойства. Растворение многих металлов в разбавленной азотной кислоте протекает с образованием водорода. Однако в свободном виде водород обычно выделяется не полностью, так как частично расходуется на восстановление избытка азотной кислоты до соединений азота более низкой валентности. [43]
В производстве аммиачной селитры обычно применяют 45 - 58 % - ную азотную кислоту. В этом случае тепловой эффект реакции нейтрализации соответственно уменьшается на величину теплоты разбавления азотной кислоты водой и на величину теплоты растворения аммиачной селитры. Количество тепла, выделяющегося при реакции, находится в прямой зависимости от концентрации и температуры азотной кислоты и газообразного аммиака. [45]
Страницы: 1 2 3 4