Разбавление - раствор - электролит
Cтраница 2
При определении коагулирующей концентрации электролита Скр нужно учитывать разбавление раствора электролита золем: концентрация его в смеси с золем вдвое меньше концентрации в добавляемом растворе. [16]
 |
Экспериментальные данные определения порогов коагуляции. [17] |
При определении коагулирующей концентрации электролита скр нужно учитывать разбавление раствора электролита золем: концентрация его в смеси с золем вдвое меньше концентрации в добавляемом растворе. [18]
ДЯИ - теплота ионизации электролита при бесконечном разбавлении; ДЯН - гипотетическое значение теплоты разбавления раствора недиссоциированного электролита до бесконечного разбавления без диссоциации; ДЯ д х - теплота разбавления, вычисленная из теории Де-бая - Хюккеля. [19]
ДЯ Ф - теплота ионизации электролита при бесконечном разбавлении; ДЯЦ - гипотетическое значение теплоты разбавления раствора недиссоциированного электролита до бесконечного разбавления без диссоциации; ДЯд х - теплота разбавления, вычисленная из теории Де-бая - Хюккеля. [20]
В работе [11] показано, что на кривых дифференциальной емкости, снятых на отдельных гранях монокристаллов серебра, наблюдались минимумы, углубляющиеся с разбавлением раствора электролита. Углубление минимумов с разбавлением указывает на их связь с изменением диффузности двойного слоя при потенциале нулевого заряда. Определенный в этих измерениях потенциал нулевого заряда для октаэдрической грани равен - 0 5 0 02 в, а для кубической - 0 65 0 02 в. Из приведенных данных Следует, что потенциал нулевого заряда поликристаллического серебра весьма близок к таковому для кубической грани монокристалла. [21]
При разбавлении раствора электролита вплоть до прекращения электростатического взаимодействия между ионами, что отвечает состоянию идеального раствора, совершается работа разрушения ионных атмосфер, которая эквивалентна работе их разряжения. Она служит мерой отличия реального раствора от идеального. [22]
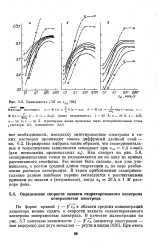 |
Зависимость / / 2 / от сэл. [23] |
Как следует из рис. 5.6, экспериментальные точки не укладываются ни на одну из кривых рассчитанного семейства. Это может быть связано, как уже упоминалось, с ростом средней длины гидратации хй по мере разбавления раствора электролита. В таком приближении экспериментальные данные наиболее хорошо согласуются с рассчитанными кривыми по модели в ( ступенька), когда х0 с 20 А в 1 М растворе фона. [24]
Если молекулы электролита и ионы, на которые они расщепляются, имеют разную окраску, при разбавлении раствора окраска смещается в сторону окраски ионов. Так, концентрированные растворы хлорной меди имеют зеленую окраску, обусловленную желтой окраской молекул СиСЬ и голубой окраской ионов Си, при разбавлении же этих растворов окраска становится голубой. С разбавлением раствора электролита степень диссоциации электролита всегда возрастает. [25]
При разбавлении раствора числитель и знаменатель дроби в выражении константы диссоциации должны измениться в равное число раз - только в этом случае сохранится постоянство величины константы. Но так как при диссоциации увеличивается число частиц, то число сомножителей в числителе больше, чем в знаменателе. Следовательно, при разбавлении раствора концентрация недиссоциированной формы уменьшается быстрее, чем концентрация диссоциированной формы, иными словами, при разбавлении растворов электролитов степень диссоциации последних увеличивается. [26]
Электролиты подразделяют на сильные и слабые. Количественно силу электролита оценивают с помощью понятия степень диссоциации, под которой понимают отношение числа молекул, распавшихся на ионы, к общему числу молекул электролита, введенного в раствор. Сильными электролитами принято считать такие, степень диссоциации которых больше 0 5, а слабыми - у которых она меньше 0 2, электролиты с промежуточными значениями степени диссоциации называют электролитами средней силы. Степень диссоциации существенно зависит от разбавления раствора электролита: в разбавленных растворах она больше. [27]
Тем не менее, выполненные этим способом вычисления получили принципиальное значение. Они показали, что нелепые результаты подсчетов теплот разбавления растворов электролитов объясняются только неточностью вычислений. [28]
В этом уравнении под знаком логарифма поставлена величина а вместо реальной концентрации с. Величину а принято называть активностью. Смысл величины активности а можно охарактеризовать, назвав ее активной концентрацией. Свободная энергия раствора сильного электролита может быть выражена уравнением ( 46) только в случае подстановки некоторой величины, не соответствующей истинной концентрации. Различие между свойствами идеального раствора и раствора сильного электролита обусловлено наличием сил взаимодействия между ионами. Силы электрического взаимодействия обратно пропорциональны квадрату расстояния между зарядами, и, следовательно, при разбавлении раствора электролита, силы взаимодействия между ионами быстро падают. Это означает, что чем раз-бавленнее раствор электролита, тем ближе он по своим свойствам к раствору идеальному. [29]
Страницы: 1 2