Разбавление - реагент
Cтраница 3
Однако на практике при проведении быстрых реакций с выделением большого количества теплоты применяют реакторы, близкие к модели идеального смешения, а не вытеснения. Причина заключается в том, что при значительной концентрации реагентов на входе в реактор вытеснения выделяется слишком много теплоты, а поэтому возможен сильный перегрев реакционной смеси и даже взрыв, например при хлорировании или нитровании органических соединений. В реакторе же смешения происходит быстрое разбавление реагентов в реакционной смеси, и процесс протекает при относительно низкой их концентрации, а следовательно, с меньшим экзотермическим эффектом в локальных точках реакционного объема. Интенсивное перемешивание также способствует эффективному съему теплоты химической реакции, например при окислении циклогексанола азотной кислотой в адипиновую кислоту. [31]
Однако возможно получить лишь один из продуктов реакции - циклический или ациклический - путем подбора соответствующих условий реакции. С другой стороны, при разбавлении реагента будет увеличиваться сольватация взаимодействующих заместителей, и тем самым они будут изолироваться друг от друга, что может приводить к некоторому снижению скорости циклизации. Однако основным фактором при циклизации является обеспечение нужной геометрии молекулы при ее переходе в циклическую структуру, а это не зависит от концентрации. Поэтому в соответствии с принципом высокого разбавления по Руггли внутримолекулярное взаимодействие облегчается по сравнению с межмолекулярным в том случае, если нужную реакцию проводить при высоком разбавлении. Этот принцип нашел важное применение в синтезе макроциклических кетонов из динитрилов по методу Циглера. Согласно этому методу, очень сильно разбавленный раствор динитрила медленно прибавляют к раствору литиевого производного вторичного амина в том же растворителе. [32]
Процессы, следующие за изменением производительности дозатора, относятся, как указывалось выше, к дозирующему тракту САДР. Этот коэффициент из физических соображений логичнее отнести к передаточной функции дозатора, но поскольку нестабильность поступающего реагента является одним из основных параметрических возмущений САДР, то переменный коэффициент Среаг удобнее вынести из звеньев, описывающих стабильную часть дозатора. Второй сомножитель в Кл - коэффициент разбавления реагента в сточной воде, который обратно пропорционален расходу Q. [33]
Сложности с применением азотсодержащих соединений начинаются при проектировании систем дозирования и раздачи реагента в котле. В отличие от аммиака и моно-этаноламина, названные в табл. 2.5 реагенты не удается перевести в газообразное состояние, поскольку при температурах плавления они начинают разлагаться, образуя высокомолекулярные соединения с повышенной температурой плавления. В связи с этим принятая в случае использования аммиака технологическая схема с разбавлением реагента паром, воздухом или дымовыми газами не может быть применена. [34]
В реакторах с холодной стенкой реагенты остаются холодными и не вступают в газофазные реакции, пока не достигнут реакционной зоны у поверхности подложки. В реакторах с горячей стенкой частицы генерируются не только за счет газофазных реакций, но и за счет осыпания пленок, осаждаемых на горячие поверхности стенок. Так как вероятность газофазных реакций пропорциональна количеству столкновений молекул реагентов, то снижение давления в реакторе или разбавление реагентов инертным газом уменьшает число таких столкновений, а следовательно, и вероятность возникновения газофазных реакций. [35]
Реагенты вводят в точке В. От точки С до точки D обычно наблюдается подъем, как это показано на рисунке, соответствующий теплоте разбавления реагента. Но может наблюдаться и спад, указывающий на то, что разбавление представляет собой эндотермический процесс ( что бывает очень редко), или на то, что температура реагента ниже, чем содержимого в сосуде для титрования. Изменение температуры ( Д71), которое можно прямо связать с изучаемой реакцией, определяют по расстоянию от точки В до точки пересечения экстраполированного отрезка CD с линией, параллельной оси абсцисс. Величина ДТ пропорциональна общему количеству выделившегося тепла ( Q - N & H), где N - число молей реагирующего вещества, а ДЯ - теплота, поглощенная молем вещества. [36]
Влияние давления ( рис. 3.3) определяется принципом Ле-Ша - телье. Если реакция идет с уменьшением объема, достижению равновесия благоприятствует давление; если реакция идет с увеличением объема, то по термодинамическим соображениям процесс можно вести при атмосферном давлении или целесообразно поддерживать в реакторе небольшое избыточное давление, чтобы не было подсоса воздуха. Когда необходим вакуум, процесс можно проводить и при атмосферном давлении для исключения подсоса воздуха, но при разбавлении реагентов инертным газом, в качестве которого чаще всего используется водяной пар. [37]
Реакторы шахтного типа являются наиболее простыми из группы контактных реакторов. Катализатор в этих аппаратах засыпан сплошным слоем. Поэтому использование таких реакторов возможно в случаях, если тепловой эфф-ект реакции невелик ил и имеется возможность снижения количества выделяющейся теплоты путем разбавления реагента инертным газом. [39]
 |
Влияние давления на ход контактного процесса. [40] |
Влияние давления ( рис. 3.3) определяется принципом Ле-Шателье. Если реакция проходит с уменьшением объема, достижению равновесия благоприятствует давление; если реакция идет с увеличением объема, то по термодинамическим соображениям процесс можно вести при атмосферном давлении или целесообразно поддерживать в реакторе небольшое избыточное давление, чтобы не было подсоса воздуха. В том случае, когда необходим вакуум, процесс можно проводить и при атмосферном давлении для исключения подсоса воздуха, но при разбавлении реагентов инертным газом, в качестве которого чаще всего используется водяной пар. [41]
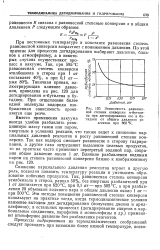 |
Зависимость равновесной степени конверсии - бутилена при дегидрировании его в бутадиен от общего давления реагентов при 860 К. [42] |
Снижение парциального давления реагентов играет и другую роль, позволяя понизить температуру реакции и уменьшить образование побочных продуктов. Так, равновесная степень конверсии этилбензола в стирол, равиая 50 %, без инертных разбавителей при 1 ат достигается при 620 С, при 0 1 ат - при 505 С, а при разбавлении 20 объемами водяного пара и общем давлении около 1 ат - при 500 С. Эти методы повышения равновесной степени конверсии используют на практике тогда, когда термодинамические условия наименее выгодны для дегидрирования ( получение диенов и арил-олефинов); в остальных процессах ( дегидрирование спиртов в карбонильные соединения, парафинов в моноолефины и др.) применяют атмосферное давление без разбавления реагентов. [43]
Добавки инертных веществ, не участвующих в реакции, должны понижать скорость процесса в замороженных растворах, поскольку они уменьшают эффект концентрирования реагентов. Концентрирование растворенных веществ в жидкой микрофазе замороженных растворов таково, что объем добавки составляет существенную часть общего объема жидкой микрофазы. Данные, полученные методам ЯМР ( см., в частности, рис. 8 13), показывают, что концентрирование происходит именно таким образом. При добавлении нитробензола эффект разбавления реагентов тоже имеет место, но константа скорости реакции в смешанном полярном растворителе существенно выше, чем в чистом бензоле или диоксане. Итак, при введении добавки нитробензола, с одной стороны, растет скорость реакции за счет увеличения полярности среды, с другой, увеличивается с ростом концентрации добавки степень разбавления реагентов в жидкой микрофазе за счет изменения ее объема. [44]
Страницы: 1 2 3 4