Величина - электронная плотность
Cтраница 1
Величина электронной плотности на реакционном центре атакуемой молекулы, которая зависит от имеющихся заместителей, их положения и структурных особенностей молекулы. Чем меньше электронная плотность ( или чем больше положительный заряд), тем больше кулоновские силы притяжения между реакционным центром молекулы и электронодонорным атакующим агентом и тем легче образуется первое переходное состояние. [1]
Величина электронной плотности на кислороде карбонильной группы, по-видимому, не так просто связана со свойствами заместителя Y. Выше говорилось, что чем выше эта плотность, тем быстрее идет водородный обмен в метильной группе производных уксусной кислоты в кислой среде. [2]
Величина электронной плотности отдельных углеродных атомов ароматического кольца, определяющаяся наличием заместителей в этом кольце, обусловливает как ориентацию вступающей интрогруппы в ядро, так и скорость этого процесса. Заместители в ядре ориентируют нитро-группу, влияя на направление передвижения NOj и степень стабильности образующегося переходного комплекса. [3]
Поскольку величина электронной плотности у реакционного центра не является определяющим фактором в радикальных реакциях ( см., например, работу [32]), то столь простая зависимость скорости рассматриваемой реакции от электронодонор-ных и электроноакцепторных свойств заместителей X не может быть понята, если считать реакцию гемолитической. [4]
Так как величина электронной плотности не является определяющим фактором при радикальных реакциях ( стр. [5]
Об этом же свидетельствуют приведенные ранее величины электронных плотностей и зарядов. [6]
Напряженность электрического поля в зоне сверхдальнего приема зависит от величины электронной плотности ионизированных слоев Ес и FZ и от мощности излучения передатчика. Для приема сигналов, отраженных от ионосферы в этой зоне, также необходимы приемники высокой чувствительности и антенны с направленным приемом. [7]
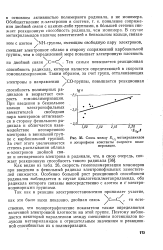 |
Связь между. 1 / 2 метакриламидов. [8] |
СС, то естественно, что полярографические показатели также определяются величиной электронной плотности на этой группе. Поэтому наблюдается некоторый параллелизм между смещением потенциалов полуволн метакриламидов к отрицательным значениям и реакционной способностью их к полимеризации. [9]
Другим способом получения информации о прочности связей в молекулярно-орбитальной теории служит исследование величины электронной плотности, создаваемой электронами различных орбиталей в различных точках пространства молекулы. Малликен [911, 915] развил подход, который получил название анализа электронных заселенностей. Большая концентрация электронной плотности в пространстве между ядрами ведет к появлению притяжения между ними. Наоборот, уменьшение электронной плотности в этой области пространства приводит к отталкиванию. [10]
Из таблицы видно, что: 1) наибольшая электронная плотность-у атома азота, 2) величина электронной плотности на атомах углерода альтернирует, 3) за исключением атомов углерода в положении 2 и 4 все остальные атомы углерода обладают значениями электронной плотности, близкими к единице Все это хорошо согласуется с химическими свойствами хинолина. [11]
Следовало ожидать, что скорость протекания полярных реакций, помимо прочих причин, зависит и от величины электронной плотности реакционного центра субстрата: высокая электронная плотность благоприятствует атаке элек-трофнльлых реагентов, а низкая электронная плотность - нуклеофнльных. [12]
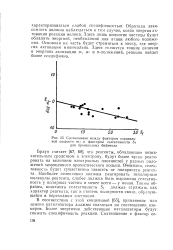 |
Соотношение между фактором парциальной скорости rrif и фактором селективности Sf для производных бифенила. [13] |
Браун считает [67, 68], что реагенты, обладающие незначительным сродством к электрону, будут более чутко реагировать на величины электронных плотностей у разных положений замещенного ароматического кольца. Очевидно, селективность будет существенно зависеть от полярности реагента. Наиболее селективно должны реагировать неполярные молекулы реагента, слабее должна быть выражена селективность у полярных частиц и менее всего - у ионов. Таким образом, константа селективности Sf должна отражать как характер реагента, так и степень полярности связи, образующейся в переходном состоянии. [14]
Такая, в сущности, чисто электростатическая трактовка реакционной способности не является теоретически доказанной, так как нет достаточных оснований считать, что величина электронной плотности в исходных молекулах полностью определяет скорость реакции. Экспериментальная проверка этой теории в настоящее время еще очень затруднительна, потому что точное распределение электронной плотности для большинства молекул неизвестно. Нередко распределение электронной плотности рассматривается достаточно произвольно, что часто приводит к необоснованным заключениям о причинах протекания тех или иных реакций. [15]
Страницы: 1 2 3