Величина - поверхность - металл
Cтраница 1
Величина поверхности металла, подлежащая защите, определяет в значительной степени расход тока, требуемого для защиты. Подземное сооружение без покрытия потребует в несколько раз больше тока, чем покрытое. Существенная разница может быть в расходе тока для защиты трубопроводов, имеющих различные покрытия. [1]
Наконец, следует отметить, что адсорбцию окиси углерода при 77 К уже давно используют для измерения величины поверхности металла в железных катализаторах синтеза аммиака [102-105], принимая Хт. Методика определения предполагает повышение давления окиси углерода до - 60 кПа, в полученные результаты вводится поправка на физическую адсорбцию. [2]
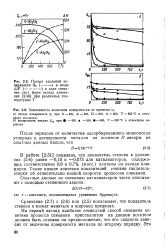 |
Потери удельной поверхности 5ь ( - - - - - - - - и воды.| Зависимость величины поверхности от времени ta. [3] |
На первый взгляд наиболее очевидный способ описания кинетики процесса спекания кристаллитов на данном носителе должен быть основан на предположении, что его скорость зависит от величины поверхности металла по второму порядку. [4]
Как показали теоретические исследования и практика, термохимический процесс со стержневым ( прутковым) магнием или электроном является более совершенным процессом по сравнению с магниевыми стружками, так как дает возможность более точно рассчитать реакцию на основе величины поверхности металла. [5]
Сущность этого метода сводится к определению изменения веса образца исследуемого металла, подвергаемого воздействию какой-либо расплавленной солевой среды в определенных условиях. При этом фиксируют и величину поверхности металла, и время ее контакта с агрессивной средой. Когда продукты коррозии полностью растворимы в солевой среде, убыль веса образца характеризует непосредственно величину разрушения металла. Однако в эксперименте это будет отвечать действительности лишь в тех случаях, когда при отмывке исследуемого образца от остатков соли не происходит какого-либо разрушения ( в том числе и механического) поверхности, а также образования на ней продуктов взаимодействия с водой и другими растворителями, которыми обрабатывался образец перед взвешиванием. Нужно помнить, что в случае химически активных металлов, таких как Zr, Hf, Ti и др., протравленная металлическая гаоиерэшоетъ весьма ре-акцио нноспособна и при контакте с воздухом покрывается окисными пленками, что может привести к ошибкам в определении истинной величины коррозии этих металлов в солевых средах. [6]
Эти оценки, вероятно, являются слегка завышенными, поскольку средний размер кристаллитов должен был несколько увеличиваться во время длительного процесса восстановления при высокой температуре, о чем свидетельствует качественное изменение мессбауэровского спектра ( см. рисунок) при повторном окислении одного из образцов. Удельная константа скорости была найдена делением начальной скорости на величину поверхности металла, определенную для каждого образца, и дана в молях бутана, образовавшегося на 1 моль бутена-1 в минуту на 1 ел2 поверхности металла. [7]
Селективная хемосорбция газов широко используется для определения различных характеристик нанесенных металлических катализаторов. Измерение количества газа, адсорбированного селективно с монослойным покрытием на поверхности металла, позволяет рассчитать величину поверхности металла и дисперсность, при условии, что известна стехиометрия хемосорбции. В каждом конкретном случае газ-адсор-бат и условия проведения эксперимента должны быть подобраны таким образом, чтобы минимизировать адсорбцию газа на носителе и обеспечить необратимую ( или слабо обратимую) хемосорбцию на металле. Одной из основных проблем селективной хемосорбции является установление истинной адсорбционной стехиометрии для данной системы металл-газ. [8]
 |
Скорость кислородной коррозии перлитной стали в зависимости от концентрации кислорода в конденсате. [9] |
Роль последних выполняет сравнительно чистая поверхность металла, имеющая беспрепятственный доступ кислорода. Анодами служат малые по площади участки металла с затрудненным доступом кислорода, например, из-за наличия на их продуктов коррозии. При катодном контроле скорость коррозионного процесса определяется величиной поверхности металла, окружающей язвы. [10]
В проточной воде стойкость испытанных сплавов алюминия с никелем и железом значительно ниже, чем в неподвижной. Состав материала при этом, вероятно, играет незначительную роль. Заметное влияние оказывает скорость течения воды, а также отношение величины поверхности металла к объему воды. При высоких скоростях воздействие уменьшается, в то время как низкое значе ние отношения поверхности металла к объему воды ( 1 - 2 см2 / л) приводит к отрицательным результатам. При этих условиях и скорости течения воды, равной 6 м / сек при 260 С, было установлено восьмикратное усиление коррозии ( по сравнению с коррозией в неподвижной воде), а также разрушение, в ряде мест, внешнего слоя. [11]
В проточной воде стойкость испытанных сплавов алюминия с никелем и железом значительно ниже, чем в неподвижной. Состав материала при этом, вероятно, играет незначительную роль. Заметное влияние оказывает скорость течения воды, а также отношение величины поверхности металла к объему воды. При высоких скоростях воздействие уменьшается, в то время как низкое значе ние отношения поверхности металла к объему воды ( 1 - 2 см2 / л) приводит к отрицательным результатам. При этих условиях и скорости течения воды, равной 6 м / сек при 260 С, было установлено восьмикратное усиление коррозии ( по сравнению с коррозией в неподвижной воде), а также разрушение, в ряде мест, внешнего слоя. [12]
Однако механизм щелевой коррозии различен при погружении металла в раствор электролита и в условиях атмосферной коррозии. Как показали работы И. К. Маршакова и И. Л. Розен-фельда, в нервом случае скорость коррозии железоуглеродистых сплавов в узких зазорах значительно ниже, чем в объеме электролита, вследствие резкого торможения катодного процесса затрудненностью доступа кислорода в зазоры. В случае контакта с металлом в объеме электролита скорость коррозии металла в зазоре определяется величиной поверхности металла, омываемой электролитом, и почти не зависит от величины зазора. Перемешивание коррозионной среды способствует усилению разрушения металлов, в частности железа, в зазорах. В атмосферных условиях коррозия в зазорах или щелях вызывается скоплением в них влаги и длительностью пребывания ее там. [13]
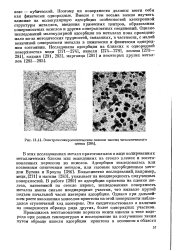 |
Электрономикроскоппческие снимки частиц металлического. [14] |
Поэтому их поверхности должны вести себя как физически однородные. Вместе с тем весьма важно изучить влияние на молекулярную адсорбцию особенностей электронной структуры металлов, введения примесных центров, образования поверхностных окислов и других поверхностных соединений. Однако исследований молекулярной адсорбции на металлах пока проведено мало из-за методических трудностей, связанных, в частности, с малой величиной поверхности металла в химически и физически однородном состоянии. [15]
Страницы: 1 2