Величина - сдвиг - потенциал
Cтраница 2
Вторую часть ячейки через 10 - 20 ч заполняют агрессивным серово-дородсодержащим раствором. Скорость диффузии водорода через стальную мембрану оценивают по величине сдвига потенциала запассивированной диффузионной стороны мембраны или по величине тока ионизации водорода на диффузионной стороне при поддержании там постоянного потенциала анодной поляризации с помощью потенциостата. [16]
Легкопассивирующиеся металлы быстро приобретают первоначальное значение потенциала после прекращения зачистки, а труднопассивирующиеся металлы - медленно. Закономерности изменения потенциала во времени при зачистке, а также величина сдвига потенциала могут в некотором отношении характеризовать поведение металла в той или иной среде и, таким образом, позволяют избежать длительных испытаний. [18]
Однако, по данным Пастернака31 и И. А. Коршунова с сотрудниками53, ацетофенон в кислых и щелочных растворах образует только одну волну. Как показали Н. А. Валяшко и Розум64, введение новых групп в кольцо ацетофенона оказывает заметное влияние на потенциал полуволны ( окси - и меток-сизамещенные ацетофенона) При этом величина сдвига потенциала зависит от того, в какое положение введена новая группа. Так, введение ОН-группыв пара-положение сдвигает потенциал полуволны к более отрицательным значениям сильнее, чем введение ее в орто-положение. [19]
 |
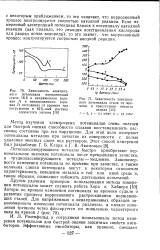
Сопоставление отношений Са / С0 и п / 0 для хромового электрода. [20] |
Данные табл. 1 позволяют сделать следующие выводы: 1) емкость двойного электрического слоя на хроме велика. Этот факт может быть объяснен тем, что в наших опытах использовался электролитический хром с бархатисто-серой поверхностью; 2) емкости С, рассчитанные из осциллограмм, снятых на хромовом электроде после катодной поляризации, значительно больше емкостей С0, рассчитанных из осциллограмм, снятых на хромовом электроде после саморастворения; 3) при одинаковой плотности тока, включавшегося при снятии осциллограмм, величины сдвига потенциала Дер, отвечавшие осциллограммам, снятым на хромовом электроде после катодной поляризации, были меньше, чем величины Дроо, отвечавшие осциллограммам, снятым на том же электроде после саморастворения. Отмеченный факт соответствует предположению об увеличении истинной поверхности хромовых электродов под влиянием больших катодных поляризаций. [21]
Значительно более эффективным методом сближения потенциалов соосаждаемых металлов является комплексообразование. Сдвиг равновесного потенциала при комплексообразовании зависит от природы металла и лиганда. Величина сдвига потенциала определяется степенью диссоциации комплексного иона. Так, осаждение сплава Си-Zn становится возможным при использовании цианидных растворов. [22]
Возможность практического использования полученного соотношения для определения деформационного изменения тока коррозии обосновывается так же, как и в известном методе снятия реальных поляризационных кривых для определения скорости коррозии металла на основе кинетической теории коррозии: идеальные поляризационные кривые, определяющие стационарный потенциал и ток коррозии, рассматриваются как продолжение тафелевских участков реальных поляризационных кривых. На рис. 66 реальные поляризационные кривые показаны сплошными линиями. Для практического расчета скорости коррозии в формулу ( 245) следует подставлять величины сдвигов потенциалов, определенные сечением реальных анодных и катодных поляризационных кривых для произвольно выбранного значения плотности тока гальваностатической поляризации в пределах тафелевских участков. [23]
Иногда из общего сдвига потенциала электрода при электролизе выделяют химическую поляризацию, к-рую связывают с процессами, изменяющими химич. Такими процессами являются: покрытие поверхности анода пленкой труднорастворимых окислов, образование сплавов и интерметаллич. Если часть сдвига потенциала электрода, обусловленная концентрационной поляризацией, может быть легко определена, напр, путем сравнения величин сдвигов потенциала при различной скорости перемешивания электролита, то разделение электрохимич. Это возрастание может быть связано как с закрытием части поверхности электрода, так и с увеличением энергии активации отдельных стадий электрохимич. [24]
Возможность практического использования полученного соотношения для определения деформационного изменения тока коррозии обосновывается так же, как и в известном методе снятия реальных поляризационных кривых для определения скорости коррозии металла на основе кинетической теории коррозии: идеальные поляризационные кривые, определяющие стационарный потенциал и ток коррозии, рассматриваются как продолжение тафелевских участков реальных поляризационных кривых. Это, очевидно, справедливо для электрохимически гомогенной поверхности, но также может быть принято для технических металлов ( железа, никеля, свинца и Др. На рис. 59 реальные поляризационные кривые показаны сплошными линиями. Для практического расчета скорости коррозии в формулу ( 232) следует подставлять величины сдвигов потенциалов, определенные сечением реальных анодных и катодных поляризационных кривых для произвольно выбранного значения плотности тока гальваностатической поляризации в пределах тафелевских участков. Из соотношения ( 229) видно, что изменение стационарного Потенциала вследствие деформации электрода не является однозначной функцией термодинамического состояния металла ( обу-словливающего анодное поведение) из-за участия катодного про-щесса. [25]
Страницы: 1 2