Величина - теплота - плавление
Cтраница 2
Теплоемкость одних и тех же веществ в жидком и твердом состоянии практически одинакова. Величина теплоты плавления зависит от состава, строения, формы и взаимного расположения структурных единиц в кристалле. [16]
Анализ кривой кристаллизации сульфолана показывает [25], что при 15 С наблюдается резкий изгиб кривой, указывающий на существование новой твердой фазы. Величины теплот плавления сульфолана при 26 и 15 С соответственно равны 2 73 и 10 6 кал / мол. Изомеры сульфолана с боковыми цепями, как правило, плавятся выше сульфолана. С увеличением числа углеродных атомов в боковой цепи температура плавления повышается. Замена алифатического или алициклического радикалов на ароматический приводит к резкому возрастанию температуры плавления. [17]
 |
Удельная теплоемкость в системе AI SO-Os - Н2О. [18] |
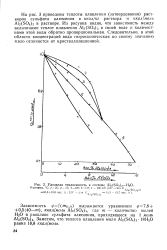
На рис 3 приведены теплоты плавления ( затвердевания) растворов сульфата алюминия в ккал / кг раствора и ккал / моль AMSOib в растворе. Из рисунка видно, что зависимость между величинами теплот плавления Al2 ( SO4) 3 в своей воде и количествами этой воды обратно пропорциональная. Следовательно, в этой области концентраций вода гигроскопическая по своему значению мало отличается от кристаллизационной. [19]
В статическом методе используется свойство силикатов сохранять аморфное состояние после плавления и быстрой закалки. Согласно термодинамической теории, тепловой запас кристаллической фазы увеличивается на величину теплоты плавления при установлении равновесия, причем в температурной функции те-плотосодержания наблюдается резкий перегиб. В точке плавления кривые удельного объема и вязкости также резко прерываются, что вызывается переходом вещества от правильной кристаллической структуры к хаотичному состоянию изотропной жидкости. [20]
 |
Уравнение Кистяковского в модификации Ветере. [21] |
Из табл. 6.5 следует, что весьма трудно получить общую корреляцию теплоты плавления с другими физическими свойствами. Добавление метильной группы может приводить как к увеличению, так и к уменьшению значений ДЯОТ, Сильно отличаются друг от друга величины теплот плавления для оптических изомеров и стереоизомеров. Различия в значениях теплот плавления ДЯт и энтропии плавления ASm разных веществ столь же велики, как и различия температур плавления, для которых не имеется каких-либо корреляций с другими свойствами. [22]
Разрыхление исходной упаковки, увеличение доступности структур /: воздействию различных реагентов находят отражение в повышении реакционной способности полимеров при различного рода гетерогенных взаимодействиях, о чем уже упоминалось в одной из предыдущих глав. Снижение степени взаимокомпенсации межмолекулярных сил в подобных разрыхленных Структурах энергетически соответствует как бы расплавленному полимеру, свободная энергия которого возрастает на величину теплоты плавления кристаллов данного полимера. [23]
Разрыхление исходной упаковки, увеличение доступности структуры к воздействию различных реагентов находят отражение в повышении реакционной способности полимеров при различного рода гетерогенных взаимодействиях, о чем уже упоминалось [811, 812] в одной из предыдущих глав. Снижение степени взаимошм-пенсации межмолекулярных сил в подобных разрыхленных структурах энергетически соответствует как бы расплавленному полимеру, свободная энергия которого возрастает на величину теплоты плавления кристаллов данного полимера. [24]
В f - Если В 0, то растворитель хороший, если В 0, то растворитель плохой. Рассчитанная по уравнению (II.1) энтальпия плавления на моль повторяющихся звеньев цепи полимера ДЯПЛ представляет собой важную внутреннюю-термодинамическую характеристику полимера, поскольку она равна количеству теплоты, необходимой для плавления одного моля кристаллических звеньев, и поэтому Д / УПЛ нельзя приравнивать к величине теплоты плавления Д / / пл, получаемой в результате прямых калориметрических исследований. [25]
О, то растворитель плохой. Рассчитанная по уравнению (II.1) энтальпия плавления на моль повторяющихся звеньев цепи полимера ДЯпл представляет собой важную внутреннюю термодинамическую характеристику полимера, поскольку она равна количеству теплоты, необходимой для плавления одного моля кристаллических звеньев, и поэтому Д / / пл нельзя приравнивать к величине теплоты плавления ДЯ Л, получаемой в результате прямых калориметрических исследований. [26]
RTIV Если В 0, то растворитель хороший, если В 0, то растворитель плохой. Рассчитанная по уравнению (II.1) энтальпия плавления на моль повторяющихся звеньев цепи полимера ДЯщ, представляет собой важную внутреннюю термодинамическую характеристику полимера, поскольку она равна количеству теплоты, необходимой для плавления одного моля кристаллических звеньев, и поэтому А / / ЙЛ нельзя приравнивать к величине теплоты плавления ДЯ Л, получаемой в результате прямых калориметрических исследований. [27]
Напротив, превращение в парообразное состояние предполагает разрыв металлической связи. Плавление и испарение металлов представляют собой совершенно разные процессы, поэтому различен и смысл, вкладываемый в понятия теплоты плавления и теплоты испарения. Величины теплот плавления металлов можно подразделить на 3 класса: в подгруппе IA она составляет 2 - 3 кДж - моль -, у остальных непереходных металлов не превышает 10 кДж - моль-1 и даже у переходных металлов, как правило, менее 20 кДж - моль-1 и лишь в редких случаях превосходит 30 кДж - моль-1. В противоположность этому минимальное значение теплоты испарения равно 70, а в ряде случаев может доходить до 800 кДж - моль-1. Приведенные в табл. 2.13 энергии, требующиеся для образования изолированных атомов, представляют собой сумму теплот плавления и испарения с поправкой на удельную теплоемкость. [28]
Можно, до известной степени, провести параллели между силами - сцепления и силами, которые удерживают в кристаллической решетке ионы гетерополярных и молекулы гомеополярных веществ. Эти силы находятся в тесной связи со строением решетки. От них зависит величина теплоты плавления и температуры плавления. [29]
Здесь A t / A Z - скорость охлаждения вблизи точки замерзания, определяемая непосредственно перед началом кристаллизации, и Zx in - - исправленное полное время кристаллизации. Если число молей веществ в обоих опытах было не одинаковым, вводится соответствующий поправочный коэффициент пр / ис - отношение чисел молей обоих веществ. Описанная методика дает величину теплоты плавления и, следовательно, идеальную криоскопиче-скую константу, ошибка при определении которой в большинстве случаев не превышает 20 % от ее величины. Точность этого опыта может быть повышена применением двух контрольных веществ, одно из которых имеет точку замерзания выше, а другое ниже данного вещества, и последующей интерполяции. [30]
Страницы: 1 2 3