Величина - энергия - диссоциация - связь
Cтраница 1
Величина энергии диссоциации связи С - С в ряду углеводородов С Н2 2 значительно ослабляется по мере увеличения числа углеродных атомов в молекуле. [1]
Хотя величина энергии диссоциации связи винил-X экспериментально не определялась, все же интересно сравнить вычисленные значения с соответствующими значениями энергии диссоциации связи этил-X. [2]
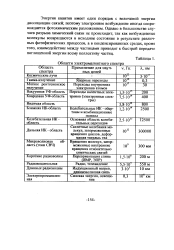 |
Области электромагнитного спектра. [3] |
Энергия квантов имеет один порядок с величиной энергии диссоциации связей; поэтому электронное возбуждение иногда сопровождается фотохимическим разложением. Однако в большинстве случаев разрыва химической связи не происходит, так как возбужденные молекулы возвращаются в исходное состояние в результате различных фотофизических процессов, а в конденсированных средах, кроме того, взаимодействие между частицами приводит к быстрой передаче поглощенной энергии всему коллективу частиц. [4]
Из энтальпий атомизации бензофуроксана и бензофуразаиа вытекает величина энергии диссоциации связи N - Ю 60 1 ккал / моль, что фактически совпадает с данными Пепекина, Лебедева и Матюшина. [5]
Из энтальпий атонизации бензофуроксана и бензофуразаиа вытекает величина энергии диссоциации связи N - Ю 60 1 ккал / ноль, что фактически совпадает с даиныни Пепекина, Лебедева и Матюшина. [6]
Интенсивности пиков ионов ( М - С1), зависящие от величины энергии диссоциации связи и стабильности образующихся ионов для СзНзС Р ( II), С3Н3С14Вг ( IV) и С3Н5С15 составляют соответственно 31 8; 19 2 и 25 8, то есть довольно близки. [7]
В рамках этой теории был проведен расчет зависимости от давления константы скорости kt, в котором величина энергии диссоциации связи С-О являлась варьируемым параметром. [8]
Авторы [127] рассчитали по энергиям связи ЛЯ /, 298 - 31 ккал / моль, однако они не сообщают, какие величины энергий диссоциации связей принимались в расчете. В измерении равновесия диссоциации окси-трифторида имеются погрешности ( см. гл. [9]
Расхождение значений энергии диссоциации бром-углеродной связи в бромтрифторметане, определенных методом электронного удара и методом Шварца, велико. Величина энергии диссоциации иод-углеродной связи в иодтрифторметане, даваемая методом электронного удара, оказывается неприемлемо низкой. Высказано мнение, что это значение ионизационного потенциала слишком велико, поэтому было предложено105 более низкое значение ( 9 3 эв), дающее лучшее совпадение значений энергии диссоциации связей в хлортрифторметане и бромтрифторметане. [10]
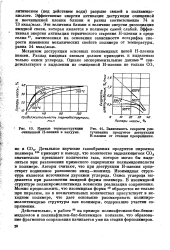 |
Кривые термодеструкции очищенной Н - пленки в вакууме.| Зависимость скорости улетучивания продуктов деструкции Н - пленки от степени превращения. [11] |
Эффективные энергии активации деструкции очищенной и неочищенной пленки близки и равны соответственно 74 и 73 ккал / моль. Эти величины близки к величине энергии диссоциации имидной связи, которая является в полимере самой слабой. Эффективная энергия активации термического старения Н - пленки в среде гелия57, вычисленная на основании зависимости логарифма скорости изменения механических свойств полимера от температуры, равна 54 ккал / моль. [12]
Прочность химической связи определяет верхний предел колебательной энергии, которой может обладать молекула, сохраняя связь ненарушенной. Поскольку колебательная энергия при нагревании возрастает, термостойкость связана с величиной энергии диссоциации различных связей. Величины энергии диссоциации связи между атомами двух элементов можно определить непосредственно, измеряя энергию диссоциации на атомы или теплоту образования из элементов. А-В по характеру подобна связям А-А и В-В, то можно ожидать, что значение энергии связи А-В будет лежать в промежутке между величинами энергий связей А-А и В-В. [13]
Главная особенность органических соединений фтора заключается в электронопритягивающем индуктивном влиянии, оказываемом сильно электроотрицательными атомами фтора и приводящем к понижению электронной плотности у соседнего реакционного центра, например карбонильной функции. Прямое доказательство такого влияния было найдено в многократно наблюдавшемся сдвиге инфракрасного поглощения карбонильной группы в сторону коротких длин волн. Лаговский получил подобные же результаты как с помощью аналогичных расчетов, так и из величины энергии диссоциации связи в соединениях CF3 - X. Хотя истинные значения электроотрицательности остаются недоступными, поскольку в измерениях такого рода нередко оказывают влияние и другие факторы3, тем не менее эти данные позволяют утверждать, что трифторметиль-ная группа притягивает электроны сильнее, чем хлор, и слабее, чем фтор. Хейзелдин и Лидэм 4 составили таблицу данных инфракрасного поглощения фторированных карбонильных соединений и подвергли ее обсуждению. [14]
Уровни вращательной энергии обычно расположены близко друг к другу, и поэтому если вращательный переход разрешен ( что не всегда имеет место), то ему соответствует низкая частота поглощенного излучения и большая длина волны. Небольшие молекулы имеют уровни вращательной энергии, разделенные промежутками примерно 1 см-г и менее, поэтому переходы наблюдаются в микроволновой области спектра. Незначительные энергии, связанные с радиочастотным излучением, могут в определенных условиях вызывать переориентацию спинов атомных ядер. Особый интерес в этом отношении представляют для органической химии ядра водорода, и случаи применения этой формы протонной спектроскопии описаны в гл. Расстояния между колебательными энергетическими уровнями по величине на несколько порядков больше, и поглощение попадает в соответственно более высокие частоты: наиболее важные колебательные полосы наблюдаются в инфракрасной области примерно между 3 и 30 мк, причем соответствующие энергетические переходы имеют величину порядка 1 - 10 ккал / моль. Электронное возбуждение требует еще больших энергий, и для большинства молекул электронные спектры проявляются только в ультрафиолетовой области. Энергия возбуждения в этом случае возрастает до 60 ккал / моль и становится того же порядка, что и величина энергии диссоциации связей; поэтому не удивительно, что электронное возбуждение часто сопровождается фотохимическим разложением. Тем не менее сложные ненасыщенные молекулы обладают достаточно низкими энергиями возбужденных состояний, и для них поглощение можно наблюдать в видимой и даже в инфракрасной областях. [15]
Страницы: 1