Величина - энергия - водородная связь
Cтраница 1
Величина энергии водородной связи - 3 кДж / моль. [1]
На основании соотношения (8.7) можно определить величину We энергии водородной связи в возбужденном электронном состоянии по сдвигу частоты инверсии v, если независимо ( например, по инфракрасному спектру поглощения) найти энергию Wg связи данного комплекса в основном электронном состоянии. Величина сдвига частоты чисто электронного перехода для поглощения ( 6v) и испускания ( 6vJ) зависит не только от разности Wg - We, но также и от разности франк-кондоновских слагаемых kwe, kwg. [2]
Для возбужденного электронного состояния наблюдаются уже иные соотношения величин энергий водородных связей в изомерных соединениях III и IV. В соответствии со сказанным выше это следует объяснить существенным перераспределением электронных плотностей на связях нафталинового ядра, происходящим при переходе из основного электронного состояния в возбужденное. [3]
 |
Температурные зависимости второго момента спектров ПМР бензола, адсорбированного цеолитами СаХ и NaX. [4] |
Энергия активации диффузии к-парафинов, оцененная по формуле У о и Федина [1] ( таблица), несколько выше энергии дисперсионного взаимодействия и имеет порядок величины энергии водородной связи. [5]
При таком выводе мы основывались на предположении, что значения свободной энергии для всех трех кристаллов одинаковы, а значения свободной энергии газов отличаются только на величину энергии водородной связи в орто-соединении. [6]
Как следует из табл. 3 и рис. 1, из различных межмолекулярных сил притяжения основную роль играют электростатические, Хотя влияние поляризации на распределение электронной плотности довольно велико, тем не менее на величине энергии водородной связи она отражается слабо. Как правило, электростатическая энергия в 5 - 7 раз превышает энергию поляризации и переноса заряда. Расчеты показывают [27], что полная энергия А. [7]
Как видно из таблицы, величины энергий водородных связей в основном электронном состоянии метиловых эфиров изомерных 1-окси - 2-нафтойной и 2-окси - 1-нафтойной кислот примерно равны друг другу, но в то же время значительно отличаются от величины энергии водородной связи в метиловом эфире 2-окси - З - нафтойной кислоты. [8]
Однако межмолекулярное взаимодействие кислот с неподвижной фазой мало изучено, так как получение термодинамических данных этих компонентов сопряжено с рядом практических трудностей. Авторами статьи сделана попытка оценить величину энергии водородной связи кислот, определяющей газохроматографиче-ское поведение этих соединений. Для этого были использованы термодинамические функции, характеризующие состояние системы: вещество - неподвижная фаза. С этой целью были определены теплоты растворения ( Hs) низших жирных кислот и некоторых углеводородов в ряде неподвижных фаз различной полярности. [9]
Если предположить, что имеется п молекул воды в растворенном кластере, тогда, по крайней мере, 2nN водородных связей должно быть разорвано при образовании одного моля активированного комплекса. Чтобы вычислить значение А / /, мы должны выбрать некоторую величину энергии водородной связи в жидкой воде. Она является наименьшей из величин энергии водородной связи, представленных в табл. 4.2. Таким образом. А / /, как минимум, равна 2 6 / 2 ккал / моль. С и уменьшается с повышением температуры, можно видеть, что молекул в мерцающем кластере п менее 4 5 / 2.6 - 1.7 при 5 С и что их число уменьшается при более высоких температурах. Поэтому, если растворение кластеров рассматривается как локальное выпаривание и если считается, что растворенные области кластеров содержат более чем одну пли две молекулы, наблюдаемые величины как АЯ, так и A S не согласуются с механизмом мерцающего кластера. [10]
Как следует из табл. 3 и рис. 1, из различных межмолекулярных сил притяжения основную роль играют электростатические. Хотя влияние поляризации на распределение электронной плотности довольно велико, тем не менее на величине энергии водородной связи она отражается слабо. Как правило, электростатическая энергия в 5 - 7 раз превышает энергию поляризации и переноса заряда. [11]
Как видно из таблицы, величины энергий водородных связей в основном электронном состоянии метиловых эфиров изомерных 1-окси - 2-нафтойной и 2-окси - 1-нафтойной кислот примерно равны друг другу, но в то же время значительно отличаются от величины энергии водородной связи в метиловом эфире 2-окси - З - нафтойной кислоты. [12]
Важно понимать, что хотя электростатическое взаимодействие частично отрицательно заряженного Е и относительно положительного Н является основным фактором образования связи, следует также учитывать другие-факторы. Благодаря относительно малому радиусу и поэтому высокой концентрации заряда атомы О, N и F могут близко подходить к ядру водорода, которое лишь слабо экранировано частично вакантной ls - орбиталью. Величины энергий водородных связей, образуемых этими элементами, зависят, конечно, от природы атома, связанного с водородом, и от молекулярного окружения этого атома, но крайние значения составляют 10 ккал / моль ( 41 87 - Ю3 Дж / моль) для фтора. Дж / моль) для азота; значение прочности Н - связи дляз кислорода имеет промежуточную величину. [13]
Если предположить, что имеется п молекул воды в растворенном кластере, тогда, по крайней мере, 2nN водородных связей должно быть разорвано при образовании одного моля активированного комплекса. Чтобы вычислить значение А / /, мы должны выбрать некоторую величину энергии водородной связи в жидкой воде. Она является наименьшей из величин энергии водородной связи, представленных в табл. 4.2. Таким образом. А / /, как минимум, равна 2 6 / 2 ккал / моль. С и уменьшается с повышением температуры, можно видеть, что молекул в мерцающем кластере п менее 4 5 / 2.6 - 1.7 при 5 С и что их число уменьшается при более высоких температурах. Поэтому, если растворение кластеров рассматривается как локальное выпаривание и если считается, что растворенные области кластеров содержат более чем одну пли две молекулы, наблюдаемые величины как АЯ, так и A S не согласуются с механизмом мерцающего кластера. [14]
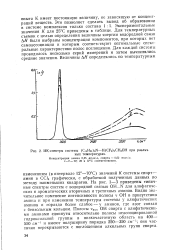 |
ИК-спектры системы ( C10H2i 3N - Н ( СР2 4СН2ОН при различных температурах. [15] |
Страницы: 1 2