Величина - свободная энергия - образование
Cтраница 1
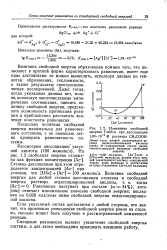 |
Изменение свободной энергии Гиббса при диссоциации. [1] |
Величина свободной энергии образования помимо того, что позволяет в краткой форме характеризовать равновесия, имеет еще одно достоинство: ее можно вычислить, используя данные по теп-лотам образования, теплоемкости, а также результаты спектроскопических исследований. [2]
Величины свободных энергий образования углеводородов из элементов при стандартной температуре 25 С 298 16 К необходимы для приближенных расчетов равновесий. [3]
Используя величины свободной энергии образования различных углеводородов из углерода и водорода, часть этих возможных путей была отвергнута с точки зрения термодинамики. [4]
Анализ величин свободной энергии образования приводит к выводу о том, что, три. [5]
Исходя из величин свободной энергии образования исходных веществ и продуктов реакции, можно вычислить константу равновесия К - Поскольку экспериментальные значения Д / 78 для алкилфенолов неизвестны, их находят расчетными методами. [6]
Известно, что величина свободной энергии образования из элементов парафинов ( начиная о этана) при температурах 400 - 500 С и выше положительна. [7]
Было установлено, что величина свободной энергии образования из элементен парафинов ( начиная с этана) при температурах 400 - 500 С и выше положительна. Это значит, что при температурах крекинга все парафины нестабильны, и термодинамически возможен их распад на элементы. Практически этот распад начинается при 700 С и выше, а вначале происходит распад связи С-С о выделением парафина и олефина и дегидрогенизация с выделением олефина и водорода. [8]
Начиная с 1250 К величина свободной энергии образования ацетилена становится меньше величин свободных энергий образования этилена и этана, что свидетельствует о возможности непосредственного получения ацетилена из углеводородов. Так, из метана ацетилен может быть получен при температурах выше 1500 К. [9]
На рис. 1 приведены величины свободной энергии образования углеводородов. [10]
Имеются ли данные о величине свободной энергии образования гидрида циркония. [11]
Рассчитанная с помощью последнего соотношения величина свободной энергии образования декагидрата равна - 1 610 ккал / моль. [12]
На рис. 9 изображена зависимость величин свободных энергий образования углеводородов от температуры; эти величины отнесены к 1 атому углерода. Зависимость от температуры исследована в пределах 700 - 1200 К. В связи с тем, что уравнения, приведенные ниже в табл. 18, будут использованы для вычислений равновесий при температурах более высоких, чем 1200 К, следует указать, что результаты, полученные экстраполированием за указанные пределы температур, нельзя считать вполне достоверными. Графический способ выражения зависимости свободной энергии образования, отнесенной к одному атому углерода, от температуры дает ясное представление об относительной стабильности индивидуальных углеводородов. [13]
Опуская результаты теории, относящиеся к вычислению величины свободной энергии образования зародышей критической величины, перейдем к определению скорости образования зародышей. [14]
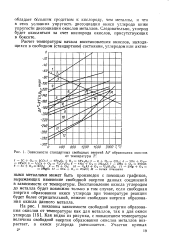 |
Зависимости стандартных свободных энергий AF образования окислов. [15] |
Страницы: 1 2 3