Величина - тепловой эффект - процесс
Cтраница 1
 |
Изменение температуры по высоте слоя катализатора при риформинге сырья с различным содержанием нафтеновых углеводородов. [1] |
Величина теплового эффекта процесса возрастает с увеличением количества образовавшихся - ароматических углеводородов и снижается с увеличением степени газообразования. [2]
Величины тепловых эффектов процессов могут различаться в миллионы раз - известны процессы с тепловыми эффектами порядка тысяч и нескольких тысячных долей килокалорий на моль. Естественно, что методики измерений разных количеств теплоты существенно различны и прежде всего различны по величине чувствительности применяемых калориметров. Правда, количества измеряемой в каждом опыте теплоты можно регулировать целесообразным выбором количеств реагирующих веществ, однако возможности такого регулирования не безграничны. [3]
Влияние температуры на равновесие системы определяется знаком и величиной теплового эффекта ДЯ процесса. [4]
Влияние температуры на равновесие системы определяется знаком и величиной теплового эффекта АЯ процесса. [5]
Согласно принципу Ле Шателье влияние температуры на равновесие определяется знаком и величиной теплового эффекта процесса. [6]
В каких случаях для определения самопроизвольности протекания процесса допустимо i пользоваться только величиной теплового эффекта процесса. [7]
Согласно принципу Ле Шателье, влияние температуры на равновесие определяется знаком и величиной теплового эффекта процесса. Объясните, почему влияние температуры определяется энтальпией процесса, а не энтропийным членом TAS, хотя повышение температуры соответствует увеличению как самого члена TAS, так и в большинстве случаев энтропии системы. [8]
Согласно принципу Ле Шателье, влияние температуры на равновесие определяется знаком и величиной теплового эффекта процесса. Объясните, почему влияние температуры определяется энтальпией процесса, а не энтропийным членом ТА5, хотя повышение температуры соответствует увеличению как самого члена TAS, так и в большинстве случаев энтропии системы. [9]
Тем не менее в большинстве случаев природу явления можно устар чить, исследовав величину теплового эффекта процесса. Очевидно, что в процессе хемосорбции выделяется значительно большее количество тепла, чем в процессе физической адсорбции. В первом случае теплота адсорбции по порядку величины близка к теплоте химических реакций, во втором - к теплоте конденсации. [10]
Известно, что согласно принципу Ле Шателье влияние изменения температуры на равновесие определяется знаком и величиной теплового эффекта процесса. Почему влияние температуры обусловлено энтальпией процесса, а не энтропийным членом 7AS, ведь повышение температуры соответствует как росту самого члена TAS, так и в большинстве случаев росту энтропии рассматриваемой системы. [11]
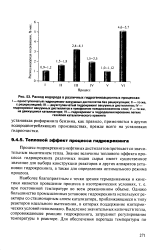 |
Расход водорода в различных гидрогенизационных процессах. I - одноступенчатый гидрокрекинг вакуумных дистиллятов без рециркуляции. II - то же. [12] |
Процесс гидрокрекинга нефтяных дистиллятов протекает со значительным выделением тепла. Знание величины теплового эффекта процесса гидрокрекинга различных видов сырья имеет существенное значение для выбора конструкции реакторов и других аппаратов установки гидрокрекинга, а также для определения оптимального режима процесса. [13]
Зависимости установлены на основании расчетов величин тепловых эффектов процесса по закону Гесса по разности энтальпий образования продуктов процесса и исходного сырья. [14]
В процессе растворения твердого кристаллического вещества энергия, - затраченная на разрушение кристаллической решетки, компенсируется выделением энергии взаимодействия молекул или ионов с растворителем. Количественное соотношение затраченной и выделенной энергии определяет знак и величину теплового эффекта процесса растворения. Например, энергия электростатического взаимодействия ионов натрия и хлора в кристалле хлорида натрия очень велика и на образование свободных ионов при разрушении одного моля NaCl потребовалось бы затратить энергию, равную 197000 калорий. Однако благодаря выделению теплоты гидратации ионов наблюдается очень малый тепловой эффект при растворении хлорида натрия. [15]
Страницы: 1 2