Разблагораживание - потенциал
Cтраница 1
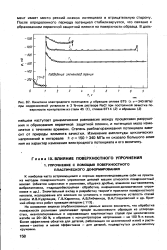
Разблагораживание потенциала, которое произошло вследствие образования трещины в начале испытания, в дальнейшем практически не изменяется вплоть до окончательного излома образца. Чем выше уровень напряжения, тем больше скорость развития трещины и тем сильнее раз-благораживается электродный потенциал. [1]
Степень разблагораживания потенциала зависит от природы элемента зачистки. [3]
О некотором разблагораживании потенциала латуни и дюралюминия в 1 н растворе NaCl 1 % HC1 по мере роста напряжений сообщает Акимов, рассматривая экспериментальные данные Кренига и Булычевой. [4]
 |
Распределение потенциалов по поверхности локального элемента медь - железо. Электролит 0 1 - н. NaCl, толщина слоя электролита 200 мкм. [5] |
Наблюдается лишь некоторое разблагораживание потенциала у границы контакта, что связано с разрушением окисной пленки, образованной на воздухе. Потенциал же катода ( меди) меняется сильно, сдвигаясь в область все более положительных значений по мере удаления от границы контакта электродов. Наиболее сильное изменение потенциала происходит вблизи контакта; с увеличением расстояния от места соединения металлов кривая приобретает все более пологий вид. [6]
Помимо этого, плавное разблагораживание потенциала во времени может быть связано с уменьшением количества деполяризатора в растворе или с торможением транспорта его к микрокатодам. [7]
При небольших толщинах полиэтиленовых пленок наблюдается более быстрое и значительное разблагораживание потенциала. С увеличением толщины полиэтиленовой пленки количество диффундирующих молекул воды становится недостаточным для заметной активизации поверхности железа. [8]
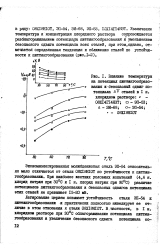 |
Влияние темаературы на потенциал литтянгообразо-ваяия и-безопасный сдвиг потенциала AV сталей в I н. хлоридном растворе. - 08Л4П4НЗТ. а - ЭП-53. Д - ЗИ-68. о - ЭП-54. - 08П8Н10Т. [9] |
Увеличение темаературы и концентрации хлоридного раствора сопровождается разблагораживанием потенциала питтингообразованяя я уменьшением безопасного сдвига потенциала всех сталей, при этом однако, отмечается определенная тенденодя к сближению сталей по устойчивости к питтингообразованию ( ряс. [10]
Подщелачивание раствора, которое способствует пассивации металлов, вызывает разблагораживание потенциала СОПфу в результате ускорения анодного процесса, так как ОН выступает в данном случае как агрессивный компонент раствора. Сдвиг потенциала; в этом случае значительно зависит от природы металла. Примерно на такую же величину смещается и потенвдал Ф2 - Здесь по сдвигу i потенциала трудно судить об изменении защитных свойств первич - д ной пленки на СОП. Из хода кривых ср-т видно, что время суще - j ствования первичной пленки на СОП увеличивается при введении в раствор 2 г / л щелочи в четыре раза для титана, железа и стали 2X13, а для стали 08XI8HIOT в 40 раз. Можно сказать, что подщелачивание способствует образованию на СОП более устойчивой защитной первичной пленки, которая, как и в случае с ингибитором Г-4, уменьшает скорость анодного процесса и увеличивает время до начала образования первых слоев оксида на СОП. Следует отметить, что подщелачивание раствора увеличивает скорость образования стационарной пассивной пленки на СОП железа более чем в 4 раза по сравнению с фоновым электролитом. Кроме того потенциал СОП железа при времени экспозиции I с положительное установившегося затем стационарного значения. На сталях 2X13 и 08XI8HIOT таких эффектов не обнаружено. [11]
Таким образом, экспериментальные кривые зависимости ускорения анодного растворения, величины разблагораживания потенциала и деформационного упрочнения от степени деформации согласуются с оценками, полученными теоретическим анализом. [12]
Механизм действия покрытий на снижение склонности стали к коррозионному растрескиванию связан с разблагораживанием потенциала стали с покрытием. [13]
Такие значения потенциала сохраняются стабильными в течение определенного времени, после чего наблюдается быстрое разблагораживание потенциала и активация металла. [14]
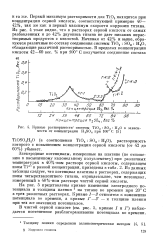 |
Кривые растворимости системы Ti02. S03. II 20 в зависимости от концентрации H2S04 при 100 С. [15] |
Страницы: 1 2 3 4