Разделение - никель
Cтраница 1
Разделение никеля, кобальта, меди и железа методом хроматографии на бумаге и их количественное определение в сульфидных рудах и породах, Журн. [1]
Процесс разделения никеля и кобальта экстракцией третичными аминами основан на способности кобальта давать анионный комплекс СоСЦ при избытке хлор-ионов. [2]
Методика разделения никеля и кобальта [1224] основана на том, что в сильнощелочной среде комплекс никеля с триэтаноламином полностью разлагается при нагревании, а комплекс кобальта устойчив. Таким образом, гидроокись никеля выделяется в осадок, а кобальт остается в растворе. [3]
Известен метод разделения никеля и кобальта при помощи этилендиампна. Трехвалентный кобальт образует растворимый этилендиаминовый комплекс при действии этилендиамина и перекиси водорода; в этих условиях никель образует малорастворимое комплексное соединение фиолетового цвета. [4]
Шустер [1117] для разделения никеля и кобальта использовал перекись водорода в щелочной среде; Гласстон и Спикман [707] - перборат натрия. [5]
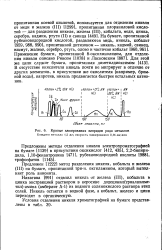 |
Кривые элюирования хлоридов ряда металлов. [6] |
Предложен [1222] метод разделения никеля, кобальта и железа ( III) на бумаге, пропитанной три-н. [7]
Весьма поучительным примером является разделение никеля ( II), кобальта ( II), железа ( III) и цинка ( II) по Краусу и Моору [67]; этот пример необходимо изучить каждому, кто собирается работать в этой области. В основе методики лежит ступенчатое элюирование из сильноосновного анионита с помощью соляной кислоты. Перед началом опыта колонку с анионитом заполняют концентрированной ( 12 М) соляной кислотой; затем вводят металлы в малом объеме ( 1 мл) концентрированного солянокислотного раствора. В этих условиях никель ( II) не удерживается анионитом и немедленно проходит через колонку. Для удаления остатков никеля колонку промывают концентрированной кислотой. Затем элюируют кобальт ( II) 4 М соляной кислотой. В этих условиях железо ( III) и цинк ( II) лишь немного перемещаются вниз по колонке. Третья стадия состоит в элюировании железа ( III) 0 5 М кислотой. [8]
Эти методы пригодны для разделения никеля и кобальта, в частности при анализе солей кобальта, содержащих небольшие количества никеля. При пропускании раствора солей никеля и кобальта с рН 5 - 6 кобальт проходит в фильтрат или легко вымывается водой, а никель остается в колонке. [9]
Применить газовую хроматографию для разделения ТФА никеля и кобальта не удалось, так как эти хелаты образуют нелетучие дигидра-ты, а при дегидратации происходит термическое разложение хелатов. [10]
Брунк, сопоставляя методы разделения никеля и кобальта, считает, что более точные результаты получаются при отделении никеля от кобальта диметилдиопсимом по сравнению с нитритным способом. Кобальт с диметилдиоксимом образует осадок зеленого цвета только при длительном стоянии. Для повышения точности результатов перед отделением осадка рекомендуется оставить стоять раствор с осадком 1 час. [11]
Рассмотренный процесс можно использовать для разделения никеля и меди с ограничениями, касающимися окислительного состояния, величины рН и концентрации анионов, но он имеет. [12]
В литературе опубликован аналогичный метод разделения никеля и кобальта на анионите ИРА-400. [13]
Дицианодиамидинсульфат [ 7201 используется также для разделения никеля и кобальта. Он осаждает никель из раствора, содержащего 10 % - ный раствор сахара. [14]
Ими также проведены опыты - по разделению никеля, кобальта, марганца, меди, и цинка. Разделение этих элементов основано на различной устойчивости анионных хлоридных комплексов в растворе соляной кислоты. [15]
Страницы: 1 2