Разделение - ионная пара
Cтраница 1
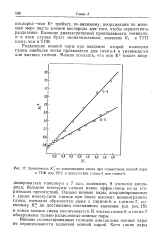 |
Зависимость / с от концентрации глима при сольватации ионной пары в ТГФ при 25 С в присутствии глима-4 или глима-5. [1] |
Разделение ионной пары при введении второй молекулы глима наиболее четко проявляется для глима-4 и уменьшается для высших глимов. [2]
Аналогичным образом влияние растворителя на & р максимально, когда разделение ионной пары начинает становиться ощутимым. [3]
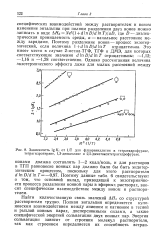 |
Зависимость lg / С - от 1 / Т для флуорениллития в тетрагидрофуране, тетрагидропиране, 1 3-диоксолане и 2 5-диметокситетрагидрофуране. [4] |
Поэтому данные табл. 6 свидетельствуют о том, что основной вклад, приводящий к экзотермично-сти процесса разделения ионной пары в эфирных растворах, вносит специфическое взаимодействие между ионом и растворителем. [5]
Если растворитель не способствует существованию свободных ионов, он тем самым дает возможность другим процессам конкурировать с процессом разделения ионной пары. Так, растворитель может атаковать ионную пару со стороны, противоположной уходящему иону Х -, приводя к образованию продукта с обращенной конфигурацией. [6]
Сохранение конфигурации наблюдается, когда амин, использованный как основание, которое отщепляет дейтерий и дает катион, способен вновь протонировать карбанион еще до разделения ионной пары ( эксп. Если протонирование по временной шкале сольватации протекает медленно, то промежуточно образующийся карбанион может оказаться в симметричном окружении, что приводит в результате к полной рацемизации ( эксп. Протонирование карбаннонов в более полярной среде и с использованием более кислых спиртов, таких как метанол или гликоль, может протекать быстро и со стороны, противоположной той, с которой осуществляется атака основанием ( эксп. Первый путь включает вращение одного из компонентов ионной пары относительно другого с последующим репротонированием третичным аммониевым противоионом. Второй путь, так называемый механизм направленного переноса, может осуществляться в тех случаях, когда в молекуле карбаниона имеются другие основные центры, с которыми третичный аммониевый противоион может образовать водородную связь. В этом случае карбанионный центр может принять плоскую конфигурацию, не теряя связи с противоионом, который далее вновь протежирует анион. [7]
 |
Зависимость К от концентрации краун-вфира [ Е ] для систем краун-эфир - Fl-Na n краун-вфир - Р1 - К в растворах ТГП и ТГФ (, воспроизведено с любезного разрешения American Chemical Society. [8] |
Величины К, К, и К2, полученные для различных систем [ 118J, находятся в соответствии с тем, что молекулы растворителя ( ТГП, ТГФ) не мешают разделению ионной пары из-за плоскостной структуры крльца краун-эфира. Таким образом, считается, что равновесие, представленное схемой (3.11), достигается в течение комцлексообразования и что тесная ионная пара образуется более легко в малополярном растворителе, в котором катион сольватируется незначительно. [9]
Значения ДЯ малы и равны - 2 5 и - 1 3 ккал / моль; значения А5 равны - 29, - 31 и - 37 знтр. Низкие значения АЯ предполагают, что монорадикал-анионная пара, по-видимому, является тесной. Специфическая сольватация, по крайней мере в 2-метил - ТГФ, по-видимому, недостаточно сильна, чтобы вызвать разделение ионной пары даже для соли лития, и, вероятно, даже в растворителях, подобных ДМЭ, не образуются в достаточной мере разделенные ионные пары. [10]
 |
Предполагаемое строение. [11] |
Модели молекул криптата показывают, что катион Ва2 прочно удерживается в клетке криптата и его вытеснение затруднено даже в воде. Поскольку катион Ва2 симметрично окружен молекулой криптата, не удивительно, что флуо-ренильный комплекс имеет в спектре только один максимум поглощения, соответствующий разделенной ионной паре. Аналогичный спектр с одним максимумом получен при добавлении; к раствору дифлуоренилбария в ТГФ этилендиамина или гекса-метилфосфортриамида. Однако неизвестно, сколько молекул комплексуется с солью бария и является ли процесс разделения ионной пары многоступенчатым. [12]
Подробных данных по этому вопросу нет, но можно предположить, что во многих случаях влияние противоиона обусловлено изменениями частотного фактора при реакции роста. Это свидетельствует о том, что противоион 1з расположен очень близко от растущего иона карбония и прочно связан с ним. Способность мономера внедряться в растущую цепь сильно затруднена. Приложенное электрическое поле увеличивает скорость и степень катиоиной полимеризации в тех случаях, когда имеется некоторое разделение ионной пары. Под действием электрического поля происходит дальнейшее увеличение расстояния между ионом карбония и его противоионом. [13]
В циклогексиламине соль лития также преимущественно находится в форме рыхлой ионной пары [45], но удивительно, что тетраметилэтилендиамин ( ТМЭДА) оказался не эффективен в образовании сольватно разделенных ионных пар. Известно, что это соединение образует сильные комплексы с литийорганическими соединениями, такими, как бутил-литий в углеводородных растворителях [33], и очень сильно увеличивает их реакционную способность. Увеличение реакционной способности приписывается усилению ионного характера связи литий - - углерод и уменьшению агрегации литийорганических соединений. Однако флуорениллитий при комнатной температуре в чистом ТМЭДА находится преимущественно в форме контактной ионной пары. Хотя этот амин должен увеличивать растворимость флуорениллития в углеводородах ( вероятно, за счет внешнего комплексования с контактной ионной парой), четыре ме-тильные группы, по-видимому, препятствуют разделению ионной пары. Приближение непосредственно к атомам азота невозможно, а следовательно, энергия взаимодействия для этого амина существенно меньше, чем для этилендиамина. В некоторых аминах наблюдаются значительные сдвиги максимумов поглощения сольватно разделенных ионных пар. При небольших размерах молекулы диамина расстояние между ионами в сольватно разделенной ионной ларе остается относительно небольшим. В то же время, как предполагал Пэскол [29], изучавший соли флуоренила в аммиаке, амины такого типа могут образовывать сольватный комплекс с карбанионом и таким образом влиять на его спектр. [14]
Страницы: 1