Разделение - электрон
Cтраница 1
Разделение электронов и дырок обеспечивается p - n - переходом. Рассмотрим его на примере кремния. При нагреве или поглощении фотона электроны могут высвобождаться, образуя при этом дырки. [2]
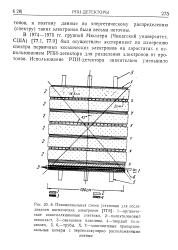
Для разделения электронов и позитронов от адронов ( в основном пионов) в установке был использован РПИ-детектор. [3]
Действительно, если принять разделение электронов на валентные и невалентные и поставить вопрос, какому варианту одноэлектронного приближения соответствуют постулаты 2 к 3, то получим следующее. [4]
Прибор позволяет также осуществлять разделение электронов по скоростям, измеряя интенсивность каждой порции электронов с данной скоростью. Энергии электронов определялись по их способности про - N, бивать препятствия, поставленные перед входом вторичного электронного умножителя. Из полученных данных ( табл. 2) следует, что первые препятствия незначительной толщины резко снижают интенсивность счета. Отсюда следует, что основная масса электронов обладает энергиями ниже 40 кэв. Увеличение толщины препятствия до 30 мк уже не влияет на интенсивность счета. [5]
В химии оказывается очень полезным разделение электронов на внешние, или валентные, и внутренние, или остов-ные. Химическая роль последних сводится к участию в формировании эффективного заряда, действующего на валентные электроны. [6]
Воря словами Бора, предположить бтчетлйвое разделение электронов в атоме на группы: с этой точки зрения разделение элементов на группы в периодической системе следует приписать постепенному образованию электронных групп в атоме по мере увеличения атомного номера [ 43, стр. В этом отношении взгляды Бора прямо коррелируют с воззрениями, развивавшимися Косселем, Льюисом, Ленгмюром и другими учеными ( например, А. [7]
Было бы, разумеется, неверным полагать, что разделение электронов на связанные и свободные носит абсолютный характер. [8]
 |
Разделение возбуждаемых светом электронно-дырочных пар на р - и-переходе. [9] |
Вентильная ( барьерная) эдс - образуется в результате разделения электронов и дырок электрич. [10]
При рассмотрении вклада электронов в простую ковалентную связь, образованную двумя атомами, можно видеть, что разделение электронов не всегда эквивалентно. Если, однако, рассматривать молекулу А-X, где А и X - различные элементы ( например, HF, IC1), то здесь, естественно, и ядра будут различны. Кроме того, атомы А и X могут сильно отличаться по своей электроотрицательности. [11]
 |
Схема электронных состояний. о - атома фтора. б - двухвалентного фторкатиона. в - аниона фтора. [12] |
Кроме рассмотренного выше процесса поляризации связи вплоть до образования свободных ионов ( гетеролиза связи) возможен и другой процесс - разделение электронов связи с образованием свободных радикалов - гомолйз связи. Углеродный атом свободного радикала обладает тремя одинаковыми заполненными орбиталями и одной одноэлектронной орбиталыо. Таким образом, он находится в состоянии р2 - гибриди-зации. [13]
В 1974 - 1975 гг, группой Мюллера ( Чикагский университет, США) [77.1, 77.9] был осуществлен эксперимент по измерению спектра первичных космических электронов на аэростатах с использованием РПИ-детектора для разделения электронов от протонов. [15]
Страницы: 1 2 3