Разделение - актинид
Cтраница 1
Разделение актинидов и очистка их от продуктов деления при помощи экстракции органическими растворителями является ярким примером решения очень сложной задачи разделения смеси элементов, принадлежащих к различным группам периодической системы элементов. Успех разделения такой смеси обеспечивается тончайшим подбором физико-химических условий проведения технологического процесса разделения. [1]
Разделению актинидов в других средах посвящено сравнительно небольшое количество работ. Все же опубликованные до настоящего времени результаты свидетельствуют о том, что аниониты в этих формах менее удобны для аналитического выделения актинидов, чем аниониты в S04 -, С1 - и NOg-формах. [2]
Метод разделения актинидов на ионообменных смолах ( катионных и анионных) наиболее пригоден для небольших количеств вещества. Этот метод будет описан ниже, так как установлено, что он дает наилучшие результаты при разделении транс-америциевых элементов. [3]
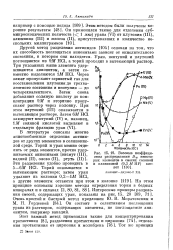 |
Весовые коэффициенты распределения Dw некоторых элементов в смесях соляной и плавиковой ( 0 3 М HF кислот, Анионит-дауэкс - 2 Х8. [4] |
Другой метод разделения актинидов [104] основан на том, что их способность поглощаться анионитами зависит от окислительного состояния, в котором они находятся. Уран, нептуний и плутоний поглощаются из 9Af HC1, а торий проходит в вытекающий раствор. Через элюат пропускают сернистый газ для восстановления плутония до трехвалентного состояния и нептуния - до четырехвалентного. Затем снова добавляют соляную кислоту до концентрации QM и вторично пропускают раствор через колонку. При этом плутоний ( III) оказывается в вытекающем растворе. [5]
Ионообменный метод оказывается полезным для разделения актинидов и во многих других случаях. [6]
Для решения вопроса о возможности применения ДТПА для разделения актинидов необходимы дополнительные исследования. [7]
Хотя по своей реакционной способности Теноилтрифторацетон близок к другим р-дикетонам, он наиболее часто применяется для разделения актинидов. [8]
С помощью теноилтрифторацетона возможна экстракция металлов из кислых растворов, что является его важным достоинством. Очень широко применяют теноилтрифторацетон для выделения и разделения актинидов. Соединения многих металлов ( урана, меди, железа и др.) с теноилтри-фторацетоном окрашены, поэтому нередко органическая фаза, содержащая теноилтрифторацетонаты этих металлов, может фо-тометрироваться. [9]
Известны многочисленные примеры использования те-ноилтрпфторацетона для разделения радиоактивных изотопов, а также осколочных элементов, образующихся в ядерном реакторе при получении расщепляющихся материалов. Наиболее широко этот дикетон применяется для выделения актиния и разделения актинидов методом экстракции. Здесь используется различная способность ионов металлов к комплексообразованию в зависимости от рН среды. R - СО - СШ - СО - - CFs и трифторацетоуксусный эфир образуют с медью, железом и другими металлами устойчивые соединения относительно высокой летучести, способные перегоняться в вакууме. Соединения с медью ( CF3COCHCOR) 2Cu окрашены в фиолетовый, синий или зеленый цвет. Еще более эффективным экстрагирующим веществом в данном случае является теноилтрифторацетон, особенно если растворителем служит не соляная кислота, а бензол. [10]
Обычно сначала проводят отделение всех лантанидов ( используемых в качестве инертных носителей, а также образующихся при получении актинидов в ядерных реакторах в качестве примесей, в числе осколков деления) от актинидов, а затем разделение актинидов. Для отделения актинидов от лантанидов колонну с катионитом после адсорбции ионов редких земель и заурановых элементов промывают или соляной, или кремнефтористоводородной ( HaSiF6) кислотами. [11]
Страницы: 1