Эмульсионное разделение
Cтраница 1
Эмульсионное разделение применяется в нефтяной промышленности главным образом для удаления примесей, содержащихся в нефти. В других областях применения эмульсионного разделения компонент, который требуется удалить, может содержаться в виде раствора в водной фазе. Примером разделения такого типа может служить удаление растворимых органических загрязнителей из промышленных сточных вод путем эмульгирования загрязненных стоков с углеводородной фазой, например бензолом. При этом загрязнители концентрируются в образующейся эмульсионной фазе и после удаления ее из системы в остающейся воде не содер-жится растворимых органических веществ. [1]
Поскольку пенное и эмульсионное разделение являются действенными способами выделения поверхностно-активных соединений, исследовались возможности использования этих процессов в нефтеперерабатывающей промышленности. Они могут быть применимы для удаления из основной массы жидкой смеси активных примесей, присутствующих в чрезвычайно малых количествах, или когда другие общеизвестные и широко применяемые процессы не обеспечивают требуемого разделения. [2]
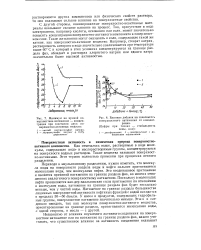 |
Минимум на кривой поверхностное натяжение - концентрация при сочетании двух поверхностно-активных веществ.| Влияние добавок на зависимость поверхностного натяжения от концентрации. [3] |
Переходя к эмульсионному разделению, нужно отметить, что молекула воды на поверхности раздела воды и нефти сильнее притягивается молекулами воды, чем молекулами нефти. Это неодинаковое притяжение и является причиной натяжения на границе раздела фаз, во многих отношениях аналогичного поверхностному натяжению. Поскольку в молекулах нефти проявляются ван-дер-ваальсовские силы притяжения по отношению к молекулам воды, натяжение на границе раздела фаз будет несколько меньше, чем у чистой воды. Натяжение на границе раздела большинства лишенных поверхностной активности нефтяных фракций с водой находится в пределах 30 - 50 дин / см. У масел и продуктов, содержащих гидрофильные группы, поверхностное натяжение значительно меньше. Этого и следовало ожидать, так как молекулы поверхностно-активного вещества, ориентированные на границе раздела, притягиваются молекулами воды, с одной стороны, и масла - с другой. [4]
Весьма сходный с эмульсионным разделением метод пытались использовать [21, 22] для выделения металлических примесей, содержащихся в нефти месторождения Норт-Белридж ( шт. При этом процессе ( рис. 5) мелкие капли водной фазы распыливали в образце нефти, создавая таким образом большую поверхность раздела нефть - вода. [5]
Для осуществления пенного или эмульсионного разделения вещество, которое необходимо выделить, должно снижать поверхностное натяжение на границе раздела фаз воздух - жидкость или вода - жидкость. Из уравнения Гиббса видно, что если наклон кривой зависимости поверхностного натяжения от концентрации ( dy / dx) велик, то на границе раздела фаз достигается высокая степень концентрирования. Следовательно, для вычисления равновесных концентраций на поверхности необходимо только измерить поверхностное натяжение растворов, содержащих различные концентрации поверхностно-активного вещества. Для большинства поверхностно-активных веществ наклон кривых зависимости поверхностного натяжения от концентрации ( dy / dx) с повышением концентрации уменьшается; таким образом, отношение избыточной концентрации на поверхности ( в пене) к концентрации в основном ядре или остаточной жидкости ( пена / ядро) с уменьшением концентрации возрастает. Однако, поскольку избыток растворенного вещества Г представляет собой, как следует из уравнения ( 7), произведение dyldx на х ( концентрация растворенного вещества), степен-ь концентрирования на поверхности или на границе раздела фаз должна зависеть не только от наклона кривой поверхностное натяжение-концентрация, но и от концентрации растворенного вещества. Гиббса, подтверждающей этот вывод, будут приведены дальше. [6]
Между растворимостью вещества или компонента, удаляемого методом эмульсионного разделения, и его эмульгирующей способностью существует некоторая зависимость; при этом следует различать молекулярную или коллоидную растворимость удаляемого компонента, а также растворимость компонента в непрерывной или в дисперсной фазе эмульсии. Имеются вполне убедительные доказательства, что в момент, когда происходит эмульгирование, активный эмульгатор может находиться-в молекулярно - или коллоиднодисперсном состоянии или даже в виде макроскопических частиц. Правило о растворимости эмульгатора в дисперсионной среде выдерживается для большинства, но не для всех эмульгаторов. В литературе указывалось [33], что не всякое вещество, растворимое как в углеводороде ( например, бензоле), так и в воде и вызывающее отчетливое снижение поверхностного натяжения на границе раздела фаз, обязательно является хорошим эмульгатором. Например, ацетон растворим в обеих этих жидкостях и все же он не бла-дает эмульгирующей способностью; не является эмульгатором и метил-этилкетон. Однако, как указывалось выше в разделах, посвященных пенному разделению, между растворимостью и поверхностной активностью существует несомненная связь. [7]
Применимость уравнения Гиббса была также экспериментально проверена при исследовании эмульсионного разделения как метода удаления ванадийпорфириновых кислот из растворов в бензоле. [8]
Эмульсионное разделение применяется в нефтяной промышленности главным образом для удаления примесей, содержащихся в нефти. В других областях применения эмульсионного разделения компонент, который требуется удалить, может содержаться в виде раствора в водной фазе. Примером разделения такого типа может служить удаление растворимых органических загрязнителей из промышленных сточных вод путем эмульгирования загрязненных стоков с углеводородной фазой, например бензолом. При этом загрязнители концентрируются в образующейся эмульсионной фазе и после удаления ее из системы в остающейся воде не содер-жится растворимых органических веществ. [9]
Гиббса для расчета концентрирования на поверхности, будет значительно больше, чем экспериментально измеренное. Уже очень давно известно, что пенное или эмульсионное разделение можно использовать как метод удаления следов примесей. [10]
Термодинамика адсорбции растворенных веществ на поверхностях раздела основывается на уравнении Гиббса [ 25.1. Это уравнение устанавливает количественную зависимость между изменениями поверхностного натяжения на границе раздела двух несмешивающихся фаз, величиной адсорбции на границе раздела и составом обеих фаз. Хотя, строго говоря, уравнение Гиббса не распространяется на динамическое пенное или эмульсионное разделение, тем не менее на нем можно основывать расчетное определение степени концентрирования, которая может быть достигнута в пенной или эмульсионной фазах. [11]
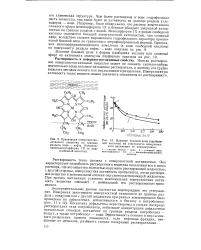 |
Влияние боковой цепи ( карбоно-вой кислоты на зависимость поверхностного натяжения от концентрации. [12] |
Иногда растворенное поверхностно-активное вещество может не снижать сколько-нибудь значительно поверхностное натяжение растворителя, и поэтому его трудно выделить методом пенного или эмульсионного разделения. [13]
Факторы, от которых зависит образование эмульсий, оказывают влияние и на разделение методом эмульсионного фракционирования. Необходимо, однако, отметить, что хотя некоторые такие факторы и обсуждаются в данной статье, автор не стремится изложить современное состояние науки об эмульсиях вообще, а ограничивается рассмотрением данных, которые могут быть использованы для усовершенствования методов эмульсионного разделения. [14]
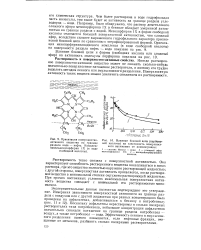 |
Влияние боковой цепи ( карбоно-вой кислоты на зависимость поверхностного натяжения от концентрации. [15] |
Страницы: 1 2