Электрохимическое разделение
Cтраница 1
Электрохимическое разделение двух металлов является проблемой, имеющей общий характер, т.е. не только применительно к электрогравиметрии. Она заключается в том, чтобы из двух металлов MI и Мг, присутствующих одновременно в растворе, лишь один выделялся на электроде. Среди различных причин, определяющих полноту осаждения и разделения, химические факторы в большей степени, чем физические, влияют на качество осадка. Их учет позволяет количественно выделить один металл в присутствии другого. [1]
Электрохимические разделения представляют особый интерес при определении следов. Они обеспечивают быстрые избирательные и легко контролируемые методы как для удаления мешающих элементов, так и для выделения или концентрирования следов элементов для последующего определения электрохимическими или другими методами. Более того, такие разделения можно часто проводить без введения дополнительных реактивов и, таким образом, свести к минимуму влияние мешающих элементов или увеличение общего количества электролита. Можно проводить электроокисление или электровосстановление, однако последнее используется в подавляющем большинстве случаев ( см., например, [270-272], а также литературу к разделу VI гл. [2]
Электрохимические разделения проводят главным образом осаждением металла, окиси или соли на поверхности электрода, часто с последующим их определением. [3]
Электрохимическое разделение молибдена и рения основано на способности Mo ( VI) электрохимически восстанавливаться до кислородных соединений молибдена с более низкими степенями окисления. Молибден полностью выделяется на катоде в виде Мо203 - zH20 за 50 - 55 мин. Оптимальными условиями электролиза являются: солянокислая среда с рН раствора 2 5, температура 40 - 45 С. Злектроосаждение молибдена проводят на матовом никелированном платиновом электроде при постоянном катодном потенциале - 0 39 в и напряжении 2 - 2 2 в. Электролит готовят следующим образом: к 120 мл раствора солей молибдена ( 50 - 100 мг) и рения ( 0 05 - 25 мг) в высших степенях окисления прибавляют 5 капель НС1 ( пл. Из этого раствора при перемешивании ( 200 - 250 об / мин) электрохимически выделяют молибден; рений при этом остается в растворе. [4]
Приемы электрохимического разделения в сочетании с радиохимическими методами были недавно описаны. [5]
При электрохимическом разделении фаз весь углерод твердого раствора и графит изолируются одновременно с карбидами в анодном осадке. В неразлагаемом осадке находятся графит и углерод твердого раствора. Раствор выпаривается, и образовавшийся осадок очищают кипящим бензолом в аппарате Сокслета. [6]
К числу химических методов относятся фракционное осаждение, соосаждение на коллекторах, применение органических реагентов-осадителей, электрохимическое разделение ( электролиз на ртутном катоде и внутренний электролиз), хроматографическое разделение, например путем ионообменной хроматографии. [7]
В связи с большими энергозатратами процесс электролиза в чистом виде не применяется сегодня для разделения изотопов водорода, а более практичными являются комбинированные методы с использованием электрохимического разделения. [8]
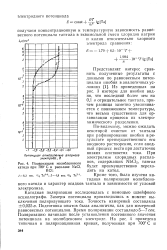 |
Поляризация молибденового. [9] |
Из приведенных на рис. 3 изотерм для ниобия видно, что последний более чем на 0 1 в отрицательнее тантала, причем разница заметно увеличивается с понижением температуры, что весьма существенно для организации процесса их электрохимического разделения. [10]
При а-распаде радиоактивного вещества, распределенного в некотором объеме, конечные продукты в виде положительных ионов собираются на отрицательно заряженной игле, давая активный осадок. Попытки электрохимического разделения - - радиоактивных изотопов были предприняты еще в первые годы зарождения радиохимии. Сул-ность этого метода состоит во введении в раствор, содержащий радиоактивный металл, электрода из другого, более электроположительного металла. При этом происходит вытеснение катионов радиоактивного металла из раствора катионами введенного металла, и на-поверхности электрода осаждается тонкий слой радиоактивного металла. Если в растворе присутствует смесь различных радиоактивных элементов, то в первую очередь будет осаждаться на введенном металлическом электроде наименее электроположительный или, как говорят, наиболее благородный из радиоактивных металлов. [12]
Определение содержания различных видов углерода в сталях и чугунах основано на их различных физических и химических свойствах и их реакциях в растворах электролитов. При электрохимическом разделении фаз весь углерод твердого раствора и графит изолируются одновременно с карбидами в анодном осадке. [13]
Этот процесс проводят на аффинажных заводах химико-термическим методом. Затем сплав подвергают электрохимическому разделению на золото и серебро ( см. с. [14]
Этот процесс проводят на аффинажных заводах химико-термическим методом. Затем сплав подвергают электрохимическому разделению на золото и серебро ( стр. [15]
Страницы: 1 2
