Полное разделение - заряд
Cтраница 2
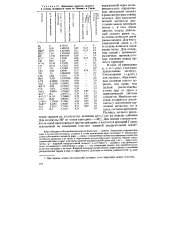 |
Дипольные моменты молекул в степень полярности связи по Полингу и Горди. [16] |
Соотношение fn / ( er) для молекул, образованных атомами одного периода, тем выше, чем дальше расположены атомы друг от друга в периодической системе элементов. Наиболее высокая полярность достигается у галогенидов щелочных металлов, но и здесь, согласно критерию Полинга, полного разделения зарядов не достигается, величина а / ( еге) все же меньше единицы. [17]
По современным представлениям связь Si-О является ковалентно-ионной с преимущественным преобладанием доли ковалентной связи. Другим доказательством значительной доли ковалентности связи Si - О является величина определенного экспериментально и рассчитанного теоретически эффективного заряда атомов кремния и кислорода в кремнеземе и некоторых силикатах. Последующими экспериментальными исследованиями и расчетами электронной структуры тетраэдрической группы [ SiO определены еще меньшие эффективные заряды на кислороде, как правило, далеко не достигающие - е -, что свидетельствует о невозможности полного разделения зарядов между кремнием и кислородом. [18]
Вследствие этого для каждого индивидуального акта роста цепи переходное состояние должно образовываться снова и снова из-за молекулярной неупорядоченности жидкой фазы. В результате кулоновского притяжения противоион будет находиться близко от заряженного конца цепи и как бы будет сопровождать растущую макромолекулу. Таким образом, в рамках кулоновского взаимодействия между заряженным концом цепи и противоположно заряженным противояоном имеется полное разделение зарядов в течение всего времени реакции роста цепи. [19]
Вследствие этого для каждого индивидуального акта роста цепи переходное состояние должно образовываться снова и снова из-за молекулярной неупорядоченности жидкой фазы. В результате кулоновского притяжения противоион будет находиться близко от заряженного конца цепи и как бы будет сопровождать растущую макромолекулу. Таким образом, в рамках кулоновского взаимодействия между заряженным концом цепи и противоположно заряженным иротивоионом имеется полное разделение зарядов в течение всего времени реакции роста цепи. [20]
На рис. 31.1 показано перемещение короткого прямого провода в магнитном поле влево. Правило правой руки предсказывает направление движения отрицательных зарядов в проводе. Сила направлена в сторону Q. Положительные заряды отталкивались бы к ближнему концу провода, а отрицательные к дальнему. Нельзя, конечно, ожидать полного разделения зарядов, так как этому препятствуют электрические силы. Положительные заряды, расположенные около Р, притягивают отрицательные, расположенные вблизи Q, и отталкивают положительные, не дошедшие до ближнего конца провода. [21]
Самопроизвольная передача электрона от металлического атома к атому неметалла в действительности вряд ли осуществляется. Для отрыва одного электрона от атома натрия требуется энергии больше, чем выделяется при присоединении его к атому хлора. Такой процесс энергетически невыгоден. Из квантовой механики также следует, что полное разделение зарядов с возникновением идеальной ионной связи А 1 В-1 никогда не может осуществиться, так как из-за волновых свойств электрона вероятность его нахождения вблизи ядра атома А может быть мала, но отлична от нуля. [22]
Ионы в молекулах не следует рассматривать как абсолютно жесткие ( неизменяемые) частицы. Под влиянием внешнего электрического поля электроны и ядра могут смещаться друг относительно друга. В этом случае происходит деформация электронных оболочек и так называемая поляризация ионов. Вещества с чисто ионной связью практически не встречаются. Даже в молекулах типа NaCl, KF невозможно полное разделение зарядов на разных атомах, и, следовательно, связь частично является ковалентной. [23]
Страницы: 1 2