Различие - концентрация
Cтраница 4
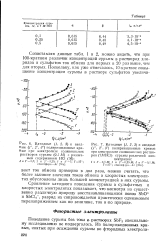
Сопоставляя данные табл. 1 и 2, можно видеть, что при 100 - нратном различии концентраций сурьмы в растворах хлоридов и сульфатов ток обмена для первых в 20 раз выше, чем для вторых. [47]
Рассмотрим систему, которая находится в неравновесном состоянии вследствие различия температуры разных участков ее или различия концентрации какого-нибудь вещества, электрического потенциала или других факторов интенсивности ( см. § 87), выравнивание которых мы назовем для сокращения общим термином обобщенной термодинамической силы и обозначим через X. [48]
В цепи (5.57) реальные потенциалы иона Х - в фазах А а В неодинаковы вследствие различия концентраций электролита MX в этих фазах. [49]
 |
Значение диффузионных потенциалов. [50] |
Величина диффузионного потенциала зависит от различия подвижностей ионов, образующих электролиты, а также от различия концентраций соприкасающихся растворов. [51]
Во многих случаях переносы количества движения и тепла происходят одновременно с переносом массы вещества, обусловленным различием концентраций компонент системы в различных ее областях. [52]
 |
Схема концентрационного элемента для измерения произведения растворимости. [53] |
Если цепь собрана из металла и раствора его соли, содержащей однозарядный катион, то при различии концентрации соли в 10 раз эдс составит 0 058 В, при концентрациях, отличающихся в 100 раз, эдс равна 0 1 16 В. При тех же условиях цепи с электролитом, содержащим двухзарядные катионы, показывают эдс в два раза, а трехзарядные - в три раза более низкие. Работа концентрационного элемента состоит в том, что металл, погруженный в более разбавленный раствор, посылает свои ионы в раствор и, таким образом, растворяется; на электроде, опущенном в более концентрированный раствор, ионы из раствора разряжаются. Таким образом, происходит выравнивание концентрации ионов в обоих электролитах, и элемент работает до тех пор, пока концентрация ионов не станет одинаковой у обоих электродов. С термодинамических представлений электрический ток вырабатывается концентрационным элементом за счет стремления системы перейти в состояние с равномерным распределением молекул и ионов во всех ее частях, т.е. в состояние с максимальной энтропией. [54]
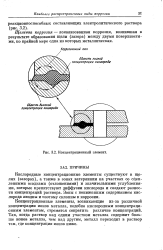 |
Концентрационный элемент. [55] |
Концентрационные элементы, возникающие из-за различной концентрации ионов металла, подобно кислородным концентрационным элементам, стремятся сократить различие концентраций. Так, когда раствор над одним участком металла содержит больше ионов металла, чем над другим, металл переходит в раствор там, где концентрация ионов ниже. [56]
Очень трудно осуществить сравнение этих данных из-за отклонений пленок S1O2 по толщине в каждом отдельном случае, различия концентрации травителей, чистоты окружающей среды и, наконец, методов обнаружения проколов. Тем не менее в любом случае совершенно очевидно, что количество проколов уменьшается при увеличении толщины слоя фоторезиста. Обычно слой фоторезиста толщиной менее 0 5 мкм не обеспечивает необходимой защиты пленки S1O2 от проникновения травителя и образования проколов. Попперт [ 1251 считает, что для того чтобы количество проколов было менее 100 см-2, необходимо, чтобы толщина слоя фоторезиста была не менее 1 мкм. [57]
 |
Схема возникновения диффузионного потенциала. [58] |
Величина диффузионного потенциала зависит, как показывает опыт, от ра &-личия подвнжностей ионов, а также от различия концентраций соприкасающихся растворов. [59]
Наблюдаемое осмотическое давление я у полиэлектролитов складывается из части пт, обусловленной макроиоиами, и другой части л обусловленной различием концентраций малых противоионов по обе стороны мембраны. Эта разность концентраций определяется равновесием Дониаиа. [60]
Страницы: 1 2 3 4