Различие - потенциал
Cтраница 1
Различие потенциалов между катодной и анодной реакциями будет возрастать, если уменьшается активность ионов металла, так как в соответствии с уравнением Нернста при этом снижается анодный потенциал. Этот же эффект легко достигается с помощью коми-лексообразующих агентов. [1]
Различие потенциалов внутри проводников создает дополнительный диффузионный поток из второго металла в первый. [2]
 |
Потенциал нулевого заряда. [3] |
Различие потенциалов нулевого заряда обусловлено тем, что существуют скачки потенциала на границе двух металлов, на границе металл вакуум и на границе металл растворнтель, не связанные с процессом перехода ионов. Разности потенциалов нулевого заряда различных металлов можно рассматривать как величины, аналогичные контактным разностям потенциалов этих металлов, измеренным в вакууме. [4]
Различие потенциалов выделения свободных металлов позволяет производить разделение катионов. [5]
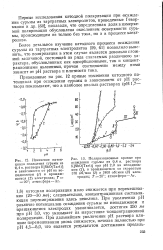
Различие потенциалов окисления ионов СГ, Вг и J ( рис. 96, справа) используется для разделения этих ионов. При действии КгСгаОт окисляется также и Вг и отгоняется в виде свободного брома. [6]
Поэтому различие потенциалов возбуждения отдельных элементов не приводит к заметному изменению чувствительности анализа. [7]
При достаточном различии потенциалов каждый из интересующих нас ионов может быть расшифрован в отдельности. Как показывает опыт, в электродной реакции могут участвовать не только ионы, но и нейтральные молекулы. [8]
При увеличении рН различие потенциалов осаждения сурьмы на неподвижном и вращающемся электродах увеличивается, достигая 250 мв при рН 3 0, что указывает на нарастание концентрационной поляризации. [10]
Предположим, что различие потенциалов жидкостного соединения при калибровке и измерениях рН, описанных в задаче 13, составляет - 0 0005 В. [11]
Метод основан на различии потенциалов восстановления п-аминобензальдегида и п-нитротолуола. [12]
Он основан на различии потенциалов восстановления фталимида и фталевого ангидрида. Фталонитрил в условиях опыта не восстанавливается. [13]
Метод основан на различии потенциалов восстановления п-аминобензальдегида и п-нитротолуола. [14]
Метод основан на различии потенциалов восстановления Аи, Си, Pd и Ag. Сначала определяют Ni на фоне 1 M NH4OH - f - 0 5 M ( NH4) 2S04 и вводят поправку на его содержание. [15]
Страницы: 1 2 3 4