Различие - взаимодействие
Cтраница 1
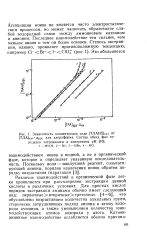 |
Зависимость концентрации соли [ ТЛАНХ ] 0рг от [ ТЛА ] 0рг - анх Для хлороформа. Состав обеих фаз определен титрованием и измерением рН ( 10. [1] |
Различие взаимодействий в органической фазе легко проявляется при рассмотрении экстракции данной кислоты в различных условиях. Для простых кислот порядок экстракции аминами обычно имеет следующий вид: первичныевторичныетретичные [4-6], что обусловлено возрастанием количества алкильных групп, стерически затрудняющих подход аниона к атому водорода аммония, а также уменьшением количества взаимодействующих атомов водорода у азота. [2]
Уточненные расчеты учитывают различия определенных торсионных взаимодействий и не обусловленных связями отталкиваний между исходными и переходными состояниями. Поэтому в такую корреляцию нужно вводить дополнительные бициклические производные. Например, для отмеченных выше производных 75 И 76 показаны нормальные скорости сольволиза. В сравнении с этим скорости сольволиза 72 ( см. выше), а также 77, 78, 79 и 80 оказываются выше такой нормы. [3]
Однако этим не исчерпывается различие взаимодействия атомов, образующих молекулу, и взаимодействия молекул. [4]
Вторичный эффект среды обусловлен различием взаимодействия ион-ион в разных растворителях, что в первую очередь определяется диэлектрической проницаемостью растворителя. Вторичный эффект среды, конечно, будет зависеть от концентрации растворенного вещества. [5]
Вторичный эффект среды обусловлен различием взаимодействия ион - ион в разных растворителях, что в первую очередь определяется диэлектрической проницаемостью растворителя. Вторичный эффект среды, конечно, будет также зависеть и от концентрации растворенного вещества. [6]
Поэтому вторичный эффект среды является мерой различия взаимодействия ион - ион в двух растворителях. Эффект среды в растворах можно определить термодинамически, если найти на опыте коэффициенты активности. Однако еще больший интерес представляет вычисление эффектов среды и определение их влияния на свойства раствора по механизму процесса. Картину механизма процесса можно представить, используя уравнение Борна и теорию Дебая - Хюккеля. [7]
Так, А.А. Предводителев [290] отмечает, что различие взаимодействия дислокаций в массивных кристаллах и в тонкой фольге вызвано уменьшением полей напряжения дислокаций в тонких кристаллах, которые вследствие близости свободных поверхностей, делаются короткодействующими... [8]
 |
Классификация методов хроматографического разделения. [9] |
Хроматографическое разделение основывается на разной относительной скорости перемещения различных частиц вдоль пути разделения из-за различия взаимодействий с неподвижной фазой и, следовательно, различного времени удерживания на ней. Полная длина пути складывается из требуемых теоретических ступеней разделения ( см. 2.2.2.1.; здесь - единиц, в которых полностью устанавливается адсорбционное или распределительное равновесие) и значения ВЭТТ. [10]
Эффект разрушения структуры связан главным образом с несоответствием формы и размера молекул неэлектролита пустотам структуры воды, а также с различием взаимодействий молекул воды с молекулами добавок и молекул воды между собой. Разрушение ведет к уменьшению упорядоченности и росту интенсивности трансляционного движения молекул. [11]
Сам акт распознавания представляет настолько универсальную функцию материи, что едва ли можно указать границу ее исчезновения, она исчезает вместе с самим веществом: элементарные частицы, атомы, молекулы распознают друг друга из-за различия взаимодействия. [12]
Наиболее общей тенденцией современных исследовний при анализе процесса фрикционного взаимодействия поверхностей с позиций физи-кохимии является рассмотрение энергетических параметров, характеризующих твердое тело и его поверхность, строение и свойства двойных электрических слоев, строение и свойства поверхностного слоя и т.п. Различия межмолеулярных взаимодействий в объемной и поверхностной фазах обусловливают избыток энергии поверхностного слоя на границе раздела фаз - поверхностную энергию, которая определяет энергетическое состояние поверхности. [13]
Второй член уравнения (V.31) выражает так называемый первичный эффект среды, характеризующий перенос иона из бесконечно разбавленного раствора в одном растворителе в бесконечно разбавленный раствор в другом. Вторичный эффект среды обусловлен различием взаимодействий ион - ион в разных растворителях, что в первую очередь определяется диэлектрической проницаемостью растворителя. Он зависит от концентрации растворенного вещества. Полный эффект среды равен сумме первичного и вторичного эффектов. [14]
Азулен представляет особый интерес ввиду необычной структуры его кристалла. Хант и Росс объясняют это различиями взаимодействия между постоянными дипольными моментами молекул в возбужденном и основном состояниях. Беспорядок в направлениях постоянных дипольных моментов дает разброс энергий перехода, и, следовательно, относительно большую ширину полосы. [15]
Страницы: 1 2