Различие - активность
Cтраница 2
Рассмотрение полученных этим методом величин ( см. табл. 26) тем не менее показывает [955, 962], что величины одних и тех же энергий связей в большинстве случаев мало зависят от метода приготовления катализатора и мало изменяются при переходе от одного металлического катализатора к другому, несмотря на различия активности этих катализаторов. Исключение составляет связь О - [ К ], прочность которой изменяется соответственно изменениям ее для связей О - К в кристаллической решетке, поскольку различие свободной энергии объемного и поверхностных соединений К-О и [ К ] - О мало. [16]
Исследование уравнения ( 1) показывает, что потенциалы разряда могут быть близкими в трех случаях: 1) если стандартные потенциалы приблизительно равны, а перенапряжения малы, 1 если стандартные потенциалы различны, но перенапряжения процесса разряда обоих катионов отличаются достаточно для того, чтобы компенсировать это различие, и 3) если разности обратимых потенциалов и перенапряжений компенсируются различием активностей ионов. Известны примеры для всех трех случаев. [17]
Не было обнаружено каких-либо признаков образования новой фазы после гидрирования, но во время гидрирования наблюдалось постепенное падение активности. Отсюда можно сделать вывод, что измеренные различия активности палладие-вых катализаторов обусловлены не только различным содержанием палладия, но и различиями структуры диспергированного металла. [18]
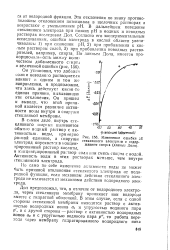 |
Изменение ошибки ДЕ стеклянного электрода с содержанием спирта ( данные Дола. [19] |
Он установил, что добавки соли и неводного растворителя влияют в одном и том же направлении, и предположил, что здесь действует какая-то единая причина, вызывающая эти отклонения. Он пришел к выводу, что этой причиной является различие активности воды внутри и снаружи стеклянной мембраны. [20]
Дол пришел к выводу, что ошибки являются следствием различия активности воды внутри и снаружи стеклянной мембраны. [21]
Из данных табл. 98 видно, что при связывании 1 1 мг кислорода наименее стойким катализатором его активность снижается почти до / 4 т первоначальной, в присутствии же более стойкого катализатора аналогичный эффект проявляется лишь после связывания катализатором 14 5 мг кислорода. Интересно, что оба катализатора до отравления кислородом одинаково активны и различия активности возникают лишь в результате отравлений, после длительного периода работы, при перегреве и под давлением. [22]
 |
Активность катализатора А при различных давлениях. [23] |
Этот катализатор, работающий при атмосферном давлении, обладает значительно меньшей активностью, чем более мелкий катализатор. Влияние размера зерен катализатора на его активность показано на рис. 91, Различие активностей катализаторов с разным размером зерен уменьшается с увеличением давления, так как при этом возрастает степень использования внутренней поверхности зерен катализатора. [24]
На основании анализа инфракрасных спектров указанных эквимолярных расплавов обсуждены и предложены возможные типы связей в соединениях, присутствующих в расплавах. Сформулирован вероятный механизм действия сульфованадатов при каталитическом окислении SO2 и рассмотрены причины различия активности катализаторов, содержащих разные щелочные металлы. [25]
Постоянство величины г ] е при повышенных скачках потенциала или градиентах потенциала означает существенное изменение химического потенциала электронов и. Это изменение величины ie, в свою очередь, означает сильное изменение концентрации электронов се, но прежде всего ( из-за различия активностей ае) также изменение состояния возбуждения. [26]
Но такой переход возможен еще и путем гидрогенизации. Хотя в этом случае и произойдет изменение состава продуктов после реакции, гидрогенизация различно замещенных этиленов, проведенная в одинаковых условиях си на одних и тех же катализаторах, позволит судить о различии активности двойных связей в разных этиленовых соединениях. Поэтому именно гидрогенизация как метод суждения о структуре непредельных соединений и была избрана Лебедевым в качестве объекта исследования. [27]
Установлено, что-при 150 наибольшей активностью обладает чистый образец германия. Образцы с сурьмой и галлием имеют активность на порядок ниже. С повышением температуры различие активностей уменьшается. [28]
Таким образом, кажется возможным, что молекула действует per se независимо от какого бы то ни было посте, пенного разложения. Далее, можно предположить, что если токсическое действие этих двух 2-фторэтиловых эфиров действительно зависит в первую очередь от всей молекулы ( в отличие от продуктов гидролиза), то такое действие может быть приписано конечным атомам фтора в молекуле; если это так, то должно 61ть какое-то оптимальное расстояние от атомов фтора для того, чтобы молекула оказывала максимальное токсическое действие. Большое значение для различия активности этиловых и 2-фторэтиловых эфиров имеет длина цепи: чем цепь короче, тем активность выше. Это различие очень мало у фторгептанкарбоксилата, а у чонан-карбоксилатов оно совершенно исчезает. [29]
Катализаторы, восстановленные при температуре около 350, содержали гексагональный а-кобальт; они весьма активны в реакции гидрирования бензола. Образцы, восстановленные при температуре выше 600, содержали почти чистые кристаллиты кубического ( J-кобальта и оказались лишенными каталитической активности. Это различие активности не может быть объяснено изменением размеров кристаллов. Возможно, что низкая каталитическая активность 3-кобальта связана с отрицательным влиянием высокой температуры восстановления, приводящей к образованию кристаллов с немногочисленными дефектами структуры. [30]
Страницы: 1 2 3