Очень большое различие
Cтраница 1
Очень большое различие в величине сил электрического и гравитационного взаимодействия наряду с одинаковой обратной квадратичной зависимостью от расстояния между частицами дает основание для гипотезы о том, что гравитационные силы появляются как следствие небольшой неточности обычной теории электрических сил. Так, Лоренц высказал предположение, что гравитационная сила возникает вследствие ничтожной раз-н-ицы между силой отталкивания между двумя частицами, обладающими зарядами одного знака, и силой притяжения между двумя частицами с одинаковыми по модулю, но противоположными по знаку зарядами. [1]
Очень большое различие между Те и Т (, характерное для большинства форм газового разряда, обусловлено громадной разницей в величине массы электронов и ионов. Внешние источники электрической энергии, с помощью которых создается и поддерживается газовый разряд, передают энергию непосредственно электронам плазмы, так как именно легкие электроны являются носителями тока. Ионы приобретают свою энергию благодаря столкновениям с быстро движущимися электронами. Однако при каждом отдельном столкновении из-за большого различия в массе легкий электрон передает иону лишь небольшую часть своей кинетической энергии, отскакивая от него, как шарик для пинг-понга, ударившийся о массивный стальной шар. [2]
Ввиду очень большого различия в ионных радиусах Fe3 и La3t ( 0 67 Аи 1 04 А) по общепринятым признакам изоморфизма следует считать соли лантана и трехвалентного железа неизоморфными. [3]
При очень большом различии в объемах окисла и металла окисная пленка разрушается вследствие больших внутренних напряжений и теряет свою сплошность. Такая окисная пленка не обладает хорошими защитными свойствами. [4]
При очень большом различии между Пп и рр необходимо учитывать заряд, создаваемый подвижными носителями в области с меньшей концентрацией основных носителей. Например, при рр пп концентрация дырок на границе п - области может превысить концентрацию доноров. [5]
При очень большом различии в объемах окисла и металла окисная пленка разрушается вследствие больших внутренних напряжений и теряет свою сплошность. [6]
При очень большом различии в электроотрицательности элементов связь между атомами носит ионный характер, при отсутствии различия - неполярный, и в промежуточном случае связь будет полярной. Обычно тем или другим способом определяют условные значения этой величины, причем результаты применения различных способов согласуются между собой в общем довольно хорошо. Пусть взаимодействуют атомы А и В и требуется определить, в каком направлении происходит перемещение электрона при этом взаимодействии. Энергия, выделяющаяся при переходе электрона от атома А к атому В, как легко видеть, равна разности между сродством к электрону Е атома В и ионизационным потенциалом / А атома А. [7]
При очень большом различии электроотрицательно-стей атомов, образующих молекулу, электронная пара почти целиком смещается к более электроотрицательному йтому. Такая связь приближается к ионной. Однако молекул, состоящих из чистых ионов, не существует. Молекулы NaCl существуют только в парообразном состоянии. [8]
При очень большом различии электроотрицательно-стей атомов, образующих молекулу, электронная пара почти целиком смещается к более электроотрицательному атому. Такая связь приближается к ионной. Однако молекул, состоящих из чистых ионов, не существует. Молекулы NaCl существуют только в парообразном состоянии. [9]
При очень большом различии электроотрицательностей атомов, образующих молекулу, электронная пара почти целиком смещается к более электроотрицательному, атому. Такая связь приближается к ионной. Однако молекул, состоящих из чистых ионов, не существует. Молекулы NaCl существуют только в парообразном состоянии. [10]
При очень большом различии электроотрицательно-стей атомов, образующих молекулу, электронная пара почти целиком смещается к более электроотрицательному атому. Такая связь приближается к ионной. Однако молекул, состоящих из чистых ионов, не существует. Молекулы NaCl существуют только в парообразном состоянии. [11]
Если учесть очень большое различие в о-в потенциалах ( или в величинах сродства к электрону) свободных галогенов, становится совершенно понятным установленный на опыте факт, что в ряду производных каждого из изученных металлов хлоросистемы обладают более высокими потенциалами, чем бромосистемы, а эти последние, - чем иодосистемы. Действительно, для иодосистем даже очень большая степень диссоциации по схеме [ PtI6 ] 2 - [ PtI4 ] 2 - Г2 не может привести к высокому значению потенциала из-за того, что нормальный потенциал системы 1а 2е - - 21 - составляет всего 0 54 в. Между тем для хлоросистем уже очень малое равновесное значение [ С12 ] достаточно для установления относительно высокого потенциала. [12]
Если учесть очень большое различие в о-в потенциалах ( или в величинах сродства к электрону) свободных галогенов, становится совершенно понятным установленный на опыте факт, что в ряду производных каждого из изученных металлов хлороспстомы обладают более высокими потенциалами, чем бромосистемы, а эти последние, - чем иодосистемы. Действительно, для иодосистем даже очень большая степень диссоциации по схеме [ PtI6 ] 2 - ч - [ PtI4 ] 2 - 12 не может привести к высокому значению потенциала из-за того, что нормальный потенциал системы I2 - j - leT 2l - составляет всего 0 54 в. Между тем для хлоросистем уже очень малое равновесное значение [ С12 ] достаточно для установления относительно высокого потенциала. [13]
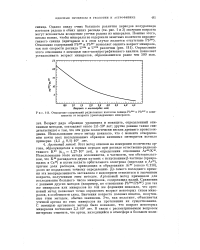 |
Отношение содержаний радиогенных изотопов свинца РЬ208 и РЬ207 в зависимости от возраста урансодержащих минералов. [14] |
Однако ввиду очень большого различия периодов полураспада изотопов радона в обеих цепях распада ( см. рис. 1 и 3) значения возраста могут искажаться вследствие утечки радона из минералов. [15]
Страницы: 1 2 3 4