Разложение - амальгама
Cтраница 1
Разложение амальгамы ведут на специальных насадках из соединений различных металлов ( циркония, вольфрама, графита), которые периодически обновляют и восстанавливают. При электролизе в раствор переходят соединения ртути, которые поступают в дальнейшем со сточными водами в окружающую среду. При производстве хлора и щелочи регенерируется далеко не все количество ртути. Это не только создает экологическую опасность, но и существенно ухудшает экономические показатели производства. При разложении амальгамы и получении раствора едкого натра образуется также некоторое количество хлоридов ртути, которые в дальнейшем попадают со щелочью в различную продукцию, например бумагу. Последняя в конечном итоге в виде отходов потребления поступает в окружающую среду. [1]
Разложение амальгамы протекает очень медленно вследствие высокого перенапряжения водорода на ней, тогда как процесс ионизации натрия происходит с большой скоростью. От скорости разложения амальгамы зависит размер аппаратов, в которых оно проводится, и количество ртути, находящейся в кругообороте. Разложение амальгамы натрия для ускорения осуществляют в ко-роткозамкнутом амальгамном элементе, в котором амальгама является анодом. Электролитом является раствор щелочи, обладающий высокой электропроводностью. Катодом служит графит, на котором разряжаются ионы водорода. Вследствие относительно низкого перенапряжения водорода на графите процесс ускоряется. Кроме того, графит не смачивается ртутью и амальгамой ( таким образом, не уменьшается перенапряжение водорода в процессе работы), не растворяется в ртути, хорошо устойчив в щелочном растворе, имеет относительно малую стоимость и хорошо поддается механической обработке. [2]
 |
Некоторые физико-химические свойства ( / - металлов II группы. [3] |
Разложение амальгам позволяет получать чистые металлы, например натрий при электролизе водных растворов NaCl с ртутным катодом. [4]
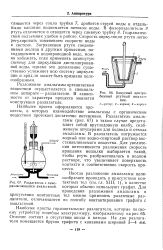 |
Конусный центробежный ртутный подъемник. [5] |
Разложение амальгамы органическим веществом осуществляется в специальном аппарате - разлагателе. В зависимости от характера процесса меняется конструкция разлагателя. [6]
Разложение амальгам, в насыщенных кислородом водных и особенно неводных средах, при интенсивном перемешивании, может привести к образованию взвешенной в растворе закиси ртути Hg2O, которая в присутствии восстановителей превращается в металлическую мелкодисперсную ртуть. Этот металлический порошок обладает большой реакционной способностью и высоким давлением паров. [7]
Разложение амальгамы является второй стадией производства хлора, щелочей и водорода по методу электролиза с ртутным катодом. [8]
Разложение амальгамы ускоряется в присутствии графита ( образование гальванической пары), поэтому на дно разлага-теля укладывают куски графита. Выход по току составляет 95 %, необходимое напряжение на электродах 4 3 - 4 7 в, расход электрической энергии 3400 - 3700 кет ч / т С12, сила тока до 500 000 а. [9]
Разложение амальгамы проводят в приборе, состоящем из газовой бюретки емкостью 25 мл, с ценой делений 0 05 мл и соединенной с ней резиновым шлангом уравнительной склянки емкостью 150 мл. В нижней части бюретки имеется сборник емкостью 10 - 15 мл, в верхней части бюретки находится воронка и трехходовой кран с боковым отводом. Трехходовой кран может соединять бюретку с воронкой или с атмосферой через боковой отвод. [10]
Разложение амальгамы представляет собой электрохимическую реакцию. Разлагатель можно рассматривать как короткозамкнутый электролизер, в котором амальгама является анодом, а графитовая насадка катодом. [11]
Разложение амальгамы, снижающее катодный выход по току, в равной мере будет снижать и анодный, так как получающаяся щелочь будет реагировать с кислым электролитом с образованием хлорноватистокислой и хлорноватокислой солей. [12]
Разложение амальгам щелочных и щелочноземельных металлов является примером сопряженных электрохимических реакций, токи обмена которых значительно отличаются друг от друга. Подобное явление наблюдается также и для ряда других систем, например при растворении свинца в серной кислоте. [13]
Разложение амальгам щелочных и щелочноземельных металлов является примером сопряженных электрохимических реакций, токи обмена которых значительно отличаются друг от друга. Подобное явление наблюдается также и в ряде других случаев, например при растворении свинца в серной кислоте. [14]
Разложение амальгам щелочных и щелочноземельных металлов является примером сопряженных электрохимических реакций, токи обмена которых значительно отличаются друг от друга. Подобное явление наблюдается также и для ряда других систем, например при растворении свинца в серной кислоте. [15]
Страницы: 1 2 3 4