Разложение - боксит
Cтраница 1
Разложение боксита производят В0 в стальном реакторе, футерованном свинцом и кислотоупорными плитками. В реактор вначале загружают 98 % - ную серную кислоту, которую разбавляют слабыми растворами от промывки шлама и нагревают до кипения. Боксит вводят в реактор периодически небольшими порциями во избежание обильного вспенивания. По окончании варки пульпа поступает в отстойники, где раствор отделяется от нерастворимых примесей. Осветленный раствор или используют непосредственно, или выпаривают с получением твердого продукта. [1]
Разложение бокситов и силикатов. Навеску пробы помещают в платиновую чашку, смачивают 3 - 5 каплями серной кислоты, приливают 5 мл фтористоводородной кислоты и выпаривают при умеренном нагревании до влажных солей. Прибавляют 0 5 - 1 0 г пиросульфата калия и сплавляют ( на горелке или в муфеле) до получения прозрачного плава. По охлаждении его растворяют в соляной кислоте ( 1: 1) и доводят этой же кислотой до объема 10 - 250 мл. [2]
Разложение бокситов и силикатов. Навеску пробы помещают в платиновую чашку, смачивают 3 - 5 каплями серной кислоты, приливают 5 мл фтористоводородной кислоты и выпаривают при умеренном нагревании до влажных солей. Прибавляют 0 5 - 1 0 г пиросульфата калия и сплавляют ( на горелке или в муфеле) до получения прозрачного плава. [3]
При разложении бокситов и силикатов навеску пробы помещают в платиновую чашку, смачивают 3 - 5 каплями концентрированной серной кислоты, приливают 5 мл фтористоводородной кислоты и выпаривают при умеренном нагревании до влажных солей. Прибавляют 0 5 - 1 0 г пиросульфата калия и сплавляют: на горелке или в муфельной печи) до получения прозрачного плава. После охлаждения его растворяют в соляной кислоте ( 1: 1) и доводят этой же кислотой до объема 10 - 200 мл ( см. стр. [4]
Определение основано на разложении боксита смесью серной и соляной кислот, выделении кремниевой кислоты из солянокислого раствора в присутствии желатина и определении диоксида кремния по разнице в массе до и после обработки фтористоводородной кислотой. [5]
В работе [62] изучено разложение высокожелезистых бокситов серной кислотой. С повышением концентрации и дозы серной кислоты извлечение этих компонентов также повышается, достигая максимальных значений при 60 % - ной концентрации кислоты и стехиометрической дозе. В качестве оптимальных рекомендованы следующие условия: концентрация H2SO4 - 60 %, доза - стехиометрическая, температура - 120 С, длительность процесса - 90 мин. [6]
Алюминат натрия NaAlO2 получается при пирогенном разложении боксита в смеси с содой и известняком по методу Ле Ша-телье - Морена. Легко растворяясь в воде, образует алюминат-ные растворы, природа к-рых до настоящего времени не вполне выяснена. В растворах средней концентрации, имеющих технич. Байера), наряду с истинно растворенным алюминатом натрия допускается также существование щелочного золя гидроокиси алюминия. Алюминатные растворы как правило крайне пересыщены и метастабилыш по отношению к устойчивой при обыкновенной t модификации гидроокиси алюминия - ги-драргилиту. Разложение растворов обусловливается старением золя А1 ( ОН) 3 и гидролитич. Оба алюмината выделены в кристаллич. [7]
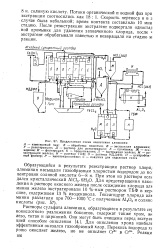 |
Предлагаемая схема извлечения алюминия. [8] |
Растворы сульфата алюминия, образующиеся в результате cej нокислотного разложения бокситов, содержат также хром, ж лезо, титан и цирконий. Они могут быть очищены перед экстра. [9]
В качестве газоочистной массы используются либо отходы производства алюминия из бокситов, остающиеся после разложения боксита щелочью, либо естественная болотная руда. [10]
Едкий натр и едкое кали. Эти плавни применяют для отделения ванадия и аллюминия от титана и железа, для разложения бокситов и в некоторых других случаях. [11]
Часто в систему необходимо вводить вспомогательные исходные вещества, например, когда новый ход процесса будет более выгодным, чем при непосредственном взаимодействии основных исходных веществ, или даже единственно возможным. В этом случае нужно так организовать производственный цикл, чтобы вспомогательное исходное вещество можно было регенерировать. После регенерации это вещество возвращается в цикл, и его расход ограничивается только потерями. Такой метод широко используется в химической технологии. Отметим, что он отличается от рециркуляции реагента, описанной на стр. Обычно возвращаемое в цикл вспомогательное исходное вещество регенерируется в результате химического превращения, а не выделяется из смеси физическими методами. Примером может служить использование концентрированной гидроокиси натрия для разложения боксита в производстве окиси алюминия методом Байера, сохранение в цикле окислов азота при башенном способе получения серной кислоты или введение в цикл аммиака при производстве соды методом Сольвея. [12]
Страницы: 1