Разложение - соль
Cтраница 1
Разложение соли в вакууме позволяет получать окисел металла с большой поверхностью. Если реакция экзотермическая, то чем ниже температура разложения соли, тем активнее катализатор. Однако во время каталитического процесса часто не удается сохранить высокую активность контакта. [1]
Разложение соли становится заметным при температурах, несколько превышающих температуру ее плавления. Одновременно происходит небольшое испарение соли. Сведений по давлению диссоциации Li2SO4 в литературе не имеется. [2]
Разложение соли на NH3, CO2 и Н2О начинается уже при 33 С. В выделяющейся воде расплываются кристаллы соли. [3]
Разложение соли производится в шнековой печи 7 в атмосфере водорода. [4]
Разложение солей водой на свободную кислоту и основание называется гидролизом. [5]
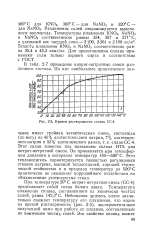 |
Кривая растворимости сплава СС-4. [6] |
Разложение солей сопровождается выделением кислорода. Теплота плавления КШ3 и МаЫО3 соответственно равна 26 4 и 45 3 ккал / кг. Для приготовления сплава применяют соли только первого сорта в соответствии с ГОСТ. [7]
Разложение соли без охлаждения или в ацетоновом растворе приводит к получению образцов с меньшей оптической чистотой. [8]
Разложение соли ж-нитрофенилдиазония производят в кругло-донной колбе. Для этого в нее помещают 20 мл воды, добавляют 25 мл концентрированной серной кислоты, полученный раствор доводят до кипения и прибавляют к нему раствор гидросульфата ж-нитрофенилдиазония. Содержимое колбы кипятят несколько минут, затем охлаждают в бане с ледяной водой. Выпавший лс-нитро-фенол отфильтровывают и перекристаллизовывают из горячей разбавленной ( 1: 1) соляной кислоты. [9]
Разложение солей 1-оксопиперидиния часто сопровождается раскрытием гетероцикла. [10]
Пиролитичеокое разложение солей кислот с целью получения альдегидов и кетонов давно и широко применяется в синтетической органической химии, но механизм реакции остается неясным. [11]
Разложение медноаммонийной соли хромовой кислоты является экзотермической реакцией и сопровождается бурным выделением газа; следовательно, для того чтобы избежать значительных механических потерь, чашки не должны быть слишком полны. [12]
Если разложение соли проводят в среде ароматического растворителя, содержащего лета-ориентирующие группы, и при этом получаются жета-замещенные продукты, то полагают, что механизм распада гетеро-литический. Образование орто - и napa - замещенных продуктов, напротив, указывает на то, что реакция протекает по радикальному механизму. [13]
Для разложения соли затрачивается тепло, что ведет к охлаждению горящей поверхности. [14]
Изучено разложение соли в области температур 50 - 100 вереде бутилового спирта и 70 - 80 в петролейном эфире. [15]
Страницы: 1 2 3 4