Разложение - природный фосфат
Cтраница 1
Разложение природных фосфатов со значительным содержанием соединений магния ( фосфориты Каратау, кингисеппские) происходит с образованием в жидкой фазе мономагнийфосфата. С увеличением степени нейтрализации ( фосфорной кислоты магнием процесс разложения фосфата сильно замедляется. Кроме того, в присутствии мономагнийфосфата увеличивается гигроскопичность суперфосфата. Более загрязненное магнием сырье подвергают обогащению. [1]
Разложение природных фосфатов азотной кислотой является первой стадией их химической переработки. При кислотном разложении фосфатного сырья содержащийся в нем фосфор извлекается ( экстрагируется) в раствор в виде фосфорной кислоты. [2]
Разложение природных фосфатов азотной кислотой является гетерогенным процессом, скорость которого определяется в основном величиной поверхности соприкосновения реагентов. При гетерогенных процессах, когда реагенты находятся в разных фазах, в реакцию будут вступать молекулы, находящиеся на поверхности раздела фаз. Следовательно, чем больше поверхность соприкосновения реагентов, тем с большей скоростью протекает процесс. Для увеличения поверхности соприкосновения фаз производится тонкое измельчение твердых веществ. [3]
Разложение природных фосфатов серной кислотой является основным технологическим процессом производства суперфосфата. В ходе этого процесса нерастворимая форма пятиокиси фосфора, содержащаяся в фосфатах, переходит в легко усваиваемую растениями растворимую форму. [4]
Разложение природных фосфатов соляной кислотой целесообразно вести по непрерывной схеме в системе, состоящей из 3 - 4 последовательно соединенных реакторов с подачей всех реагентов в первый реактор. Реакционная пульпа содержит очень небольшое количество нерастворимого остатка, который отделяется в сгустителе. Сгущенную пульпу фильтруют, осадок промывают водой в промывных сгустителях, на фильтрах или центрифугах. [5]
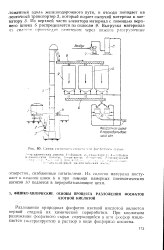 |
Схема силосного скллтл тля гЬггфлтппго сн ья. [6] |
Разложение природных фосфатов азотной кислотой является первой стадией их химической переработки. При кислотном разложении фосфатного сырья содержащийся в н - - м фосфор извлекается ( экстрагируется) в раствор в виде фосфорной кислоты. [7]
Разложение природных фосфатов азотной кислотой проводится непрерывным способом в нескольких последовательно соединенных реакторах, расположенных каскадом. Азотнокислотная вытяжка самотеком переходит из одного реактора в другой. В каждом реакторе имеется мешалка, непрерывно перемешивающая реагенты. Реакторы и мешалки изготовляют из хромоникелевой стали. [8]
Разложение природных фосфатов, содержащих з аметные количества соединений магния ( фосфориты Каратау, кингисеппские), происходит с образованием в жидкой фазе мономагнийфосфата. С увеличением степени нейтрализации фосфорной кислоты магнием процесс разложения фосфата сильно замедляется. Более загрязненное магнием сырье подвергают обогащению. [9]
Обычна разложение природных фосфатов ведут при температуре 45 - 50 С, которая является оптимальной. При уменьшении температуры ниже 45 С разложение замедляется. С повышением температуры выше 50 С уменьшается вязкость раствора, улучшаются условия диффузии и скорость разложения увеличивается. Однако усиливается коррозия аппаратуры. Требуемая температура поддерживается главным образом за счет теплового эффекта реакции ( 290 кДж / моль); при необходимости подогревают или охлаждают в теплообменнике азотную кислоту. [10]
Обычно разложение природных фосфатов ведут при температуре 45 - 50 СС, которая является оптимальной. При уменьшении температуры, ниже 45 СС разложение замедляется. С повышением температуры уменьшается вязкость раствора, улучшаются условия диффузии вещества и скорость разложения увеличивается. Однако выше 50 С усиливается коррозия аппаратуры. Требуемая температура ( 45 - 50 С) поддерживается главным образом за счет теплового эффекта реакции; температуру азотной кислоты, которая должна составлять 30 С, регулируют подогревом или охлаждением кислоты в теплообменнике. [11]
Обычно разложение природных фосфатов ведут при температуре 45 - 50 С, которая является оптимальной. При уменьшении температуры ниже 45 разложение замедляется. С повышением температуры уменьшается вязкость раствора, улучшаются условия диффузии вещества и скорость разложения увеличивается. Однако выше 50 резко усиливается коррозия аппаратуры. Требуемая температура ( 45 - 50) поддерживается главным образом за счет теплового эффекта реакции; температуру азотной кислоты, которая должна составлять 30 С, регулируют подогревом или охлаждением кислоты в теплообменнике. [12]
Обычно разложение природных фосфатов ведут при температуре 45 - 50 С, которая является оптимальной. [13]
Скорость разложения природных фосфатов серной кислотой возрастает с повышением температуры. На рис. 35 показано изменение степени разложения фосфорита серной кислотой во времени при различных температурах. При 90 С фосфорит разлагается практически полностью менее чем за 30 мин Апатитовый концентрат разлагается с относительно меньшей скоростью чем осадочные фосфориты, но его разложение также ускоряется при повышении температуры. [14]
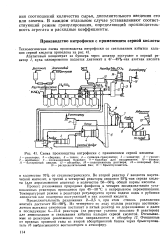 |
Схема производства нитрофоски с применением серной кислоты. [15] |
Страницы: 1 2 3 4