Разложение - гидрат - окись
Cтраница 1
Разложение гидрата окиси метилциклопропилметйлтриметил-аммония дает триметил-амин и свыше 70 % выхода. [1]
Для объяснения механизма разложения гидратов окиси четвертичных соединений аммония Ханхарт и Ингольд предположили наличие ионизации атома водорода у - углерода; по их представлению в дальнейшем он теряет свои валентные электроны, соединяясь с гидроксильной группой с образованием воды. [2]
Следует также учитывать, что разложение гидрата окиси рутения - экзотермическая реакция, в результате которой могут произойти механические потери рутения. Во избежание потерь следует восстановить гидра-тированную окись до наступления бурной экзотермической реакции. Это достигается добавлением в раствор мацерированной бумаги. Иногда для этой цели смачивают осадок сернокислым аммонием, однако не всегда это предотвращает распыление осадка. [3]
 |
Рентгенограммы конечных продуктов 38. реакции активного кремнезема с известью. На рентгенограмме. [4] |
Остановки при 550, отвечающей разложению гидрата окиси кальция, не наблюдается. [5]
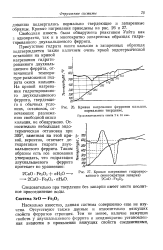 |
Кривая нагревания гидратиро. [6] |
Присутствие гидрата окиси кальция в запаренных образцах подтверждается также наличием очень яркой эндотермической остановки на кривой нагревания гидрати-рованного двухкальциевого феррита, отвечающей температуре разложения гидрата окиси кальция. [7]
 |
Общий вид блока. [8] |
Сопоставление результатов определения давления диссоциации Са ( ОН) 2 динамическим и статическим методами может служить доказательством того, что, в отличие от аналогичного процесса диссоциации гидроокиси магния, при разложении гидрата окиси кальция сразу же образуется окись кальция стабильной структуры независимо от скорости протекания реакции. [9]
 |
Прибор для получения аммиака. [10] |
Для каждой данной температуры ( при постоянном давлении) в системе устанавливается определенное равновесие. Повышение температуры смещает равновесие влево-в сторону разложения гидрата окиси аммония, а-при понижении температуры равновесие. [11]
Взаимодействие окиси кальция с двуокисью углерода начинается при 350 С и ускоряется при повышении температуры. Значительная скорость достигается при 600 С и выше. Водяные пары ускоряют рекарбонизацию при температуре ниже температуры разложения гидрата окиси кальция и незначительно замедляют ее выше этой температуры. [12]
Образование олефинов вместо спиртов ( например, бутилен - f - - f - вода, вместо бутилового спирта) рассматривалось Брауном как доказательство того, что спирт не является промежуточным продуктом данной реакции. Исходя из представления о поведении спиртов при повышенных температурах, последняя точка зрения кажется вполне обоснованной. Однако, метильный радикал не единственный, отщепляющийся в виде спирта; из гидратов окисей октил - и цетил-триметиламмония образуется не только октилен, но и октиловый спирт и, соответственно, не один цетилен, но и цетиловый спирт. Аналогичным образом гептиловый спирт сопровождает гептилен при разложении гидрата окиси гептилтриметиламмония. Таким образом, трудность образования углеродных цепей с двойной связью на концах цепи возрастает с удлинением цепи. Является ли такое положение общим правилом, ответить трудно до проведения достаточного количества опытов. [13]
У одних материалов ( доломита, известняка, мрамора) воздействие огня вызывает хим. разложение, другие материалы ( алюминий) плавятся, третьи ( бетон, гранит, сталь) деформируются. Так, бетон под воздействием высокотемпературного пламени частично теряет прочность от внутренних напряжений, возникающих вследствие различия температурного коэфф. Кроме того, при т-ре выше 500 С начинается разложение гидрата окиси кальция в структуре цементного камня. [14]
Страницы: 1