Каталитическое разложение - аммиак
Cтраница 1
Каталитическое разложение аммиака на металлических поверхностях представляет собой яркий пример специфичности действия катализаторов, так-как эта реакция на поверхности вольфрама имеет нулевой порядок и на ее скорость не влияет ни один из продуктов реакции. Это означает, что достаточно учитывать только первый член в знаменателе уравнения ( 21) и что поверхность катализатора всегда покрыта адсорбированными молекулами, а поэтому скорость реакции полностью определяется скоростью, с которой эти молекулы покидают поверхность. [1]
Каталитическое разложение аммиака должно проходить те же ступени в обратном порядке с наиболее медленной десорбцией азота. [2]
Рассмотрим, например, реакцию каталитического разложения аммиака на металлах. Принято считать, что этот процесс контро-руется десорбцией азота, адсорбированного на поверхности катализатора. [3]
Благодаря очень низкой равновесной концентрации NH3 каталитическое разложение аммиака можно легко изучать при атмосферном давлении. [4]
В обоих способах для восстановления применяется водород, получаемый каталитическим разложением аммиака и отличающийся высокой чистотой. [5]
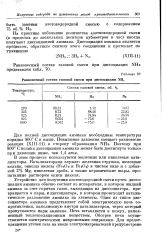 |
Равновесный состав газовой смеси при диссоциации NH3. [6] |
Устройство для получения азотоводородной смеси путем диссоциации аммиака обычно состоит из испарителя, в котором жидкий аммиак за счет горячих газов, выходящих из диссоциатора, превращается в пары, и диссоциатора, в котором происходив каталитическое разложение аммиака на элементы. Один из типов диссоциатора аммиака представляет собой электрическую печь сопротивления, наполненную внутри катализатором, через который пропускаются пары аммиака. Печь вставляется в кожух, наполненный теплоизоляционным веществом. Обогрев печи осуществляется электрическими нихромовыми спиралями. [7]
Наблюдаемые зависимости удовлетворительно объясняются следующими предположениями о сущности каталитического окисления аммиака: реакция идет в сторону образования окиси азота при взаимодействии молекул аммиака с адсорбированным на поверхности катализатора кислородом, находящимся в активном состоянии; образующийся активный комплекс, в состав которого входят аммиак и кислород, способен быстро окисляться кислородом до окиси азота и воды; элементарный азот образуется в результате каталитического разложения аммиака. [8]
В некоторых каталитических реакциях образующиеся частицы могут адсорбироваться более сильно, чем реагирующий газ. Это происходит в случае каталитического разложения аммиака на платине при 1000 С. [9]
На первый взгляд может показаться, что роль поверхности в каталитической реакции сводится просто к изменению энергии активаций реакции на величину теплоты адсорбции. Например, истинная энергия каталитического разложения аммиака на вольфраме составляет всего 39 икал / моль, тогда как энергия активации реакции в газовой фазе равна 90 кка л / моль. [10]
Направлению реакции в сторону образования элементарного азота благоприятствуют: понижение содержания кислорода в газовой смеси, чрезмерное повышение или понижение температуры, отравление катализатора, удлинение времени пребывания газа в аппарате при неизменных прочих условиях. Все это позволяет считать образование азота результатом каталитического разложения аммиака на поверхности катализатора, свободной от кислорода, в том числе и на поверхности стенок контактного аппарата до зоны катализа. Это предположение тем более вероятно, что разложение аммиака на платиновом катализаторе в отсутствие кислорода протекает со скоростью, сравнимой со скоростью окисления аммиака на том же катализаторе. [11]
Оно выражает соотношение между константой скорости реакции К. Уравнение Срикан-тана было подтверждено данными, полученными Гиншельвудом для каталитического разложения аммиака на вольфраме и разложения закиси азота на платине. В узком интервале температур выражение 3 / 2 lg Т можно рассматривать как константу, и тогда уравнение превращается в уравнение Аррениуса. Сравнивая термоэлектрическую эмиссию для различных поверхностей ( табл. 7), Срикантан пришел к выводу, что каталитическая активация газов должна быть приписана электронной эмиссии каталитической поверхности. [12]
Страницы: 1