Дальнейшее разложение - фосфат
Cтраница 2
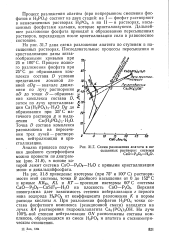 |
Схема разложения апатита в насыщенных растворах системы СаО - Р2О5 - Н2О. [16] |
Процесс разложения апатита ( при непрерывном смешении фосфатов и Н3РО4) состоит из двух стадий: на I - фосфат растворяют в ненасыщенных растворах Н3РО4, а на II - в растворах, насыщенных фосфатами кальция, которые кристаллизуются. Дальнейшее разложение фосфата приводит к образованию пересыщенных растворов, переходящих после кристаллизации соли в равновесное состояние. [17]
Большим недостатком камерного способа, как и в производстве простого суперфосфата, является необходимость длительного складского вылеживания и дообработки продукта. Дальнейшее разложение фосфата в схватившейся массе протекает весьма медленно и ведется в течение длительного времени. Помимо недостаточного использования фосфата, значительных затрат на сооружение громоздких складов, расхода труда и энергии на периодическое перемешивание продукта, при складском дозревании суперфосфата выделяются загрязняющие атмосферу фтористые газы, уловить которые практически невозможно. [18]
В таком растворе невозможно растворение фосфата. Использование такого раствора для дальнейшего разложения фосфата возможно лишь после выделения из него части кальция. После этого раствор фосфорной кислоты оказывается ненасыщенным по отношению к фосфатам кальция и способен растворять дополнительное количество фосфата. [19]
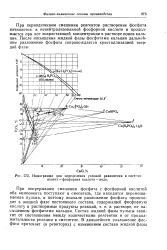 |
Номограмма для определения условий равновесия в системе апатит - фосфорная кислота - вода. [20] |
При периодическом смешении реагентов растворение фосфата начинается в ненейтрализованной фосфорной кислоте и продолжается при все возрастающей концентрации в растворе ионов кальция. После насыщения жидкой фазы фосфатами кальция дальнейшее разложение фосфата сопровождается кристаллизацией твердой фазы. [21]
В таких растворах, несмотря на малое содержание в них Р2О5, происходит дальнейшее достаточно интенсивное разложение фосфата. Жидкая фаза, образующаяся при использовании концентрированной кислоты, является насыщенным фосфорными солями инкон-груэнтным раствором, в котором дальнейшее разложение фосфата идет с очень малой скоростью, к тому же непрерывно уменьшающейся вследствие кристаллизации продукта реакции на поверхности зерен фосфата. Отсутствие этого явления при использовании разбавленной кислоты является дополнительным положительным фактором, облегчающим диффузию кислоты к поверхности частиц фосфата. [22]
При оптимальном составе фосфатного комплекса ( точки в и е, когда коэффициент разложения апатита достигает - 60 %, наступает затвердевание суперфосфатной пульпы. Это еще более замедляет реакцию. Дальнейшее разложение фосфата вынужденно ведется в течение многих дней на складе. [23]
По мере разложения апатита концентрация Н3Р04 постепенно уменьшается. Состав раствора в начале кристаллизации находится в точке пересечения луча кристаллизации, проведенного из точки N через точку данного состава фосфатного комплекса, с соответствующей ветвью изотерм. При дальнейшем разложении фосфата происходит выпадение моно - или дикальцийфосфата или их смесей. [24]
Температура и концентрация вводимой в процесс серной кислоты мало влияют на химический состав продукта, но сильно отражаются на его структуре и физических свойствах. При высоких температурах и концентрациях серной кислоты сульфат кальция кристаллизуется быстро и оседает на поверхности зерен фосфата в виде плотной корки. Это замедляет дальнейшее разложение фосфата. [25]
Дальнейшее разложение фосфата во второй стадии происходит при взаимодействии его с насыщенным раствором и сопровождается выделением твердой фазы. Данные о равновесии в системе могут быть использованы для выбора условий кристаллизации твердой фазы того или иного состава. При образовании в первой стадии насыщенных эвтонических растворов, отвечающих по своим составам узловым точкам, дальнейшее разложение фосфата ( если оно возможно было бы по кинетическим условиям) сопряжено с выделением в твердую фазу вначале смеси моно - и дикальцийфосфата, а к концу процесса - одного дикальцийфосфата. В точках s или Sj ( в зависимости от нормы Н3РО4) в равновесных условиях разложение апатита полностью заканчивается. Степень нейтрализации жидкой фазы по мере выделения твердой фазы на ветви монокальцийфосфата повышается, а на ветви дикальцийфосфата - уменьшается. Повышение температуры уменьшает степень нейтрализации на ветвях дикальцийфосфатэ увеличивает ее на ветвях монокальцийфосфата. [26]
 |
Состав камерного суперфосфата. [27] |
Чтобы избежать быстрого затвердевания реакционной массы, продолжительность смешения фосфата с серной кислотой должна быть не более 7 мин. В результате этого в процессе смешения природные фосфаты успевают прореагировать с серной кислотой лишь в незначительной степени. Дальнейшее разложение серной, а затем фосфорной кислотой происходит без перемешивания массы в камерах, где суперфосфат выдерживается 1 - 2 ч для дальнейшего разложения фосфата и затвердевания. При этом одновременно кристаллизуются фосфаты кальция. [28]
В начальный период - до образования насыщенного раствора - вся масса фосфорной кислоты реагирует с небольшой частью фосфата. Весовое отношение между кислотой и реагирующим фосфатом Ж: Т составляет - 20 - 4 - 50: 1 ( в зависимости от концентрации и температуры кислоты), затем в течение некоторого времени твердая фаза выделяется в небольшом количестве с образованием подвижной - текучей пульпы. По мере дальнейшего разложения фосфата и увеличения количества твердой фазы масса ( загустевающая пульпа) постепенно густеет, пока не схватится в сплошной твердый монолит. [29]
С этой целью сульфат или бисульфат аммония вводят в реакционную массу в процессе разложения апатита азотной кислотой, а не после завершения этого процесса. В этом случае, образующийся при разложении фосфата азотной кислотой нитрат кальция сразу же взаимодействует с сульфат-ионом. Кальций с самого начала процесса выводится из сферы реакции в виде осадка сульфата кальция, и химическая активность жидкой фазы все время остается высокой. После того как азотная кислота израсходуется, дальнейшее разложение фосфата идет за счет ненасыщенной соединениями кальция фосфорной кислоты. Находящийся в растворе нитрат аммония ( образовавшийся в результате взаимодействия сульфата аммония с нитратом кальция) не тормозит, в отличие от нитрата кальция, разложение апатита слабой фосфорной кислотой. [30]
Страницы: 1 2 3