Размер - комплексный ион
Cтраница 1
Размер комплексного иона в кристаллах различных солей исключительно постоянен. Способ упаковки комплексных ионов в кристалле также определяется геометрическими требованиями: их относительным общим размером и, естественно, относительным числом ионов каждого вида. [1]
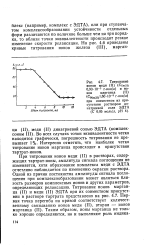
С другой стороны, увеличение размера комплексного иона сказывается на уменьшении коэффициента диффузии. В данном случае оба эти фактора, действующие в противоположных направлениях, не вызывают изменения коэффициента диффузии комплексного иона. [2]
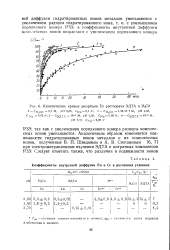 |
Кинетические кривые десорбции Ей растворами ЭДТА и HsCit.| Коэффициенты внутренней диффузии Ей и Се в различных условиях. [3] |
РЗЭ, так как с увеличением порядкового номера размеры комплексных ионов уменьшаются. Аналогичным образом изменяются подвижности гидратированных ионов металлов и их комплексных ионов, полученные В. П. Шведовым и А. В. Степановым Г6, 7 ] при электромиграционном изучении ЭДТА и цитратных комплексов РЗЭ. [4]
Следует иметь некоторое представление об общей форме и размере обычных комплексных ионов. [5]
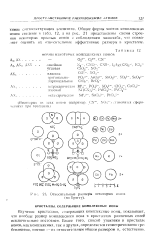 |
Относительные размеры некоторых ионов ( по Брэггу. [6] |
Изучение кристаллов, содержащих комплексные ионы, показывает, что вообще размер комплексного иона в кристаллах различных солей исключительно постоянен. [7]
При уменьшении диэлектрической проницаемости смешанного растворителя эти константы возрастают, однако величина эффекта меньше найденного при аналогичном изучении констант диссоциации. Указанное влияние диэлектрической проницаемости было объяснено на основе изменения размера комплексных ионов. [8]
 |
Схематическое распределение комплексных ионов в растворе в зависимости от концентрации лигандов. 1 - [ М ]. 2 - [ ML ]. 3 - [ ML2 ]. 4 - [ ML3 ]. 5 - [ MU ]. [9] |
Последовательное взаимодействие полярных молекул МНз с ионом [ Си ( НзО) 4 ] не приводит к столь резкому изменению значения Ki, так как размер заряда иона сохраняется: Ki 1 4 10; 2 3 2 10; Хз 7 7 10 л / моль. Уменьшение значения KI в этом случае вызвано постепенным увеличением размеров комплексного иона и изменениями конфигурации внутренней сферы. [10]
При титровании ионов меди ( II) в растворах, содержащих тартрат-ионы, амплитуда сигнала поглощения не изменяется, хотя образование комплекса меди с ЭДТА отчетливо наблюдается по изменению окраски раствора. Одной из причин постоянства амплитуды сигнала поглощения при комплексообразовании может являться близость размеров комплексных ионов и других параметров, определяющих релаксацию. [12]
Гидратация ( некоординационная) галогенидных и аквагалоге-нидных комплексов зависит от их состава ( заряда), размера и симметрии. Для смешанных аква - и гидроксогалогенидных комплексов большое значение имеет гидратация за счет образования водородных связей между координационно связанными молекулами воды или ионами гидроксила с молекулами растворителя. При прочих равных условиях гидратация уменьшается с увеличением размера комплексного иона. Симметричные октаэдрические и тет-раэдрические комплексные ионы обычно не имеют больших ди-польных моментов и поэтому при прочих равных условиях гидра-тированы слабее. Смешанные аквагалогенидные и гидроксогало-генидные комплексы имеют более низкую симметрию и из-за дипольного момента они гидратированы сильнее. Вероятно, цпс-комплексы гидратируются больше, чем соответствующие транс-комплексы. [13]
В том случае, когда при смешении расплавленных солей образуется новый комплексный ион, изотерма электропроводности становится сложнее. Многочисленный экспериментальный материал по этому вопросу был получен А. Г. Бергманом и его сотрудниками. Они установили следующее: если компоненты образуют химическое соединение, то его удельная электропроводность меньше, чем наиболее электропроводного из них. Это объясняется тем, что размеры нового комплексного иона больше, а его подвижность меньше. [14]
Страницы: 1