Размер - атом
Cтраница 1
Размер атома не может быть указан точно. Это обусловлено тем фактом, что расстояние между ядром и электроном не фиксировано, а может меняться. Тем не менее, как отмечалось выше, вероятность нахождения электрона вдали от ядра очень мала. [1]
Размер атома может быть определен различными способами, но обычно используется рентгеноструктурный анализ. Результаты таких исследований доказывают, что размер атома уменьшается слева направо в данном периоде периодической системы элементов и увеличивается сверху вниз в каждой группе элементов периодической системы. [2]
Размер атома определяется радиусом наиболее удаленной от ядра электронной орбиты. [3]
Размеры атомов весьма незначительны. Так, радиус атома водорода равен 0 53 - Ю-8 см, ли 0 53 А. [4]
Размеры атомов этих элементов соответственно меньше, чем элементов группы О - Ро, а сродство к электрону значительно больше, чем элементов группы кислорода. [5]
Размеры атомов и молекул не превышают обычно нескольких ангстремов. Например, диаметр атома водорода равен 1 А, молекула водорода имеет диаметр приблизительно 2 6 А, а молекула кислорода - 3 2 А. [6]
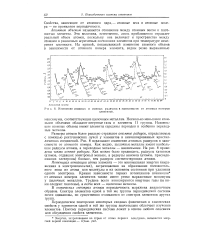 |
Изменение атомных и ионных радиусов в зависимости от атомных номеров. [7] |
Размеры атомов более реально отражают атомные радиусы, определяемые с помощью рентгеновских лучей у элементов и неионизированных кристаллических соединений. Как видно, щелочные металлы имеют наибольшие радиусы атомов, а переходные металлы - наименьшие. На рис. 8 приведены также ионные радиусы. [8]
 |
Электростатическая машина. [9] |
Размеры атомов и элементарные заряды весьма малы. [10]
Размеры атомов, в свою очередь, влияют на их свойства. Так, например, атомы элементов лития Li, натрия Na, калия К обладают наибольшими размерами по сравнению с атомами других элементов в тех же периодах. В связи с этим наружные электроны в атомах щелочных металлов находятся дальше от ядра, слабее притягиваются к нему и могут легко удаляться. При переходе в периодах от типичных металлических элементов к галогенам размеры атомов уменьшаются, сила притяжения наружных электронов к ядру увеличивается, что и приводит к уменьшению восстановительных и увеличению окислительных свойств. [11]
Размеры атомов О и F очень близки. [12]
Размеры атомов также оказывают существенное влияние. [13]
Размеры атома соизмеримы с длиной волны излучения, применяемого в рентгеноструктурном анализе. [14]
Размеры атомов и ионов определяются размерами электронной оболочки. Но по квантовомеханическим представлениям электронная оболочка не имеет строго определенных границ. Практически используют вычисленные по экспериментальным данным значения радиусов атомов и ионов, находящихся в соединении. Различают ковалентные радиусы и металлические радиусы атомов. [15]
Страницы: 1 2 3 4