Размер - кристалл - платина
Cтраница 1
Размер кристаллов платины в АПК оказывает значительное влияние на активность платиновых катализаторов в реакциях превращения углеводородов. [1]
По данным [440], размер кристаллов платины зависит от среды, в которой проводится предварительная термическая обработка до 500 С. В атмосфере азота получаются большие кристаллы, чем в водороде или на воздухе. При последующем восстановлении он разлагается с формированием мелких кристаллов платины. В токе водорода восстановление начинается при более низ-них температурах ( 250 - 300 С), что также способствует получению высокодисперсной платины. С комплекс разлагается с образованием металлической платины, частицы которой при высоких температурах легко диффундируют по поверхности носителя и агрегируют в крупные кристаллы. Если катализатор восстановлен, то при обработке на воздухе укрупнение частиц платины идет в 2 раза интенсивнее, чем в азоте. С увеличением парциального давления кислорода эффект спекания платины возрастает. [2]
Пористая структура носителя оказывает влияние и на размер кристаллов нанесенной платины. Увеличение внутренней поверхности носителя способствует повышению дисперсности осаждаемой на нем платины и, соответственно этому, росту каталитической активности, отнесенной к единице веса платины. [3]
Влияние среды, в которой проводится термообработка до восстановления водородом, на размеры кристаллов платины отмечалось и для металлцеолитных катализаторов, приготовленных пропиткой, что связано с образованием различных соединений металлов, отличающихся подвижностью и способностью восстанавливаться водородом. [4]
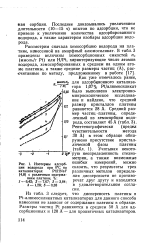 |
Изотермы адсорб. [5] |
Как уже отмечалось ранее, ммопьНг для адсорбционного катализа-тора 1 07 % Pt / алюмосиликат 0 гз было выполнено электронно-микроскопическое исследование и найдено, что средний 02 размер кристаллов платины равняется 28 А. [6]
 |
ТПВ оксида платины в катализаторе Pt-ALO., 1188 ]. [7] |
Показано [196], что повышение температуры от 300 до 500 С при обработке водородом катализатора Pt / Al2O3 ( предварительно восстановлен 500 СС, затем окислен О2 450 С), приводит к значительному снижению хемосорбционной емкости платины по водороду, измеряемой отношением Н: Pt. Размер кристаллов платины при этом не увеличивается, что было установлено с помощью электронной микроскопии. Явление это, однако, обратимо, и первоначальное значение Н: Pt можно получить, обработав катализатор кислородом при 450 С и проведя восстановление водородом при 30Q С. [8]
В работе [297] также показано, что хлорирование алюмоплатиновых катализаторов четыреххлористым углеродом в окислительной или инертной среде сопровождается образованием таких интермедиатов, как фосген и летучие хлориды платины. Обработка АПК четыреххлористым углеродом в токе водорода ведет к незначительному увеличению размеров кристаллов платины, а в случае использования газообразного НС1 дисперсность платины не изменяется. [9]
Боресков с сотрудниками [24, 26] исследовал каталитическую активность различных платиновых катализаторов ( платину в виде проволоки и сетки, губчатую платину, платинированный силика-гель) в реакции окисления двуокиси серы. Было найдено, что удельная активность ( поверхность платины определялась адсорбцией) приблизительно одинакова для всех исследованных образцов и в очень малой степени зависит от размеров кристаллов платины и предварительной температурной обработки образцов. Энергия активации реакции окисления S02 на массивной платине и на платинированном силикагеле составляет 23 3 0 6 ккал / молъ. Каталитическая активность платинированного силикагеля на единицу веса платины остается приблизительно постоянной при изменении концентрации платины от 0 001 до 0 5 %; Следовательно, размеры кристаллов платины в платинированном силикагеле не зависят от концентрации платины и определяются только структурой пор силикагеля и предварительной тепловой обработкой. Каталитическая активность в реакции окисления S02 была определена для платины, вольфрама, золота, сплавов платина - золото, хрома, рубидия и серебра. Оказалось, что серебро каталитически неактивно. Все другие металлы, за исключением платины, имеют приблизительно одинаковую активность, однако меньшую, чем у платины. Херт [61] применил особый метод расчета для нахождения соотношения между данными по окислению S02 на платиновых катализаторах. [10]
На гладкие подложки из пирографита и золота электроосаждением наносили платину в таком количестве, чтобы она занимала лишь часть поверхности носителей. На этих электродах изучены адсорбция водорода, метанола, муравьиной кислоты, а также электрохимическое выделение водорода и электроокисление метанола и муравьиной кислоты. Показано, что размер кристаллов платины и степень заполнения подложек катализатором влияют на удельную каталитическую активность платины, поверхность которой рассчитывали по адсорбции водорода. Повышение удельной каталитической активности с уменьшением заполнения носителей катализатором объясняется увеличением доли участия носителя в исследованных реакциях. [11]
Боресков с сотрудниками [24, 26] исследовал каталитическую активность различных платиновых катализаторов ( платину в виде проволоки и сетки, губчатую платину, платинированный силика-гель) в реакции окисления двуокиси серы. Было найдено, что удельная активность ( поверхность платины определялась адсорбцией) приблизительно одинакова для всех исследованных образцов и в очень малой степени зависит от размеров кристаллов платины и предварительной температурной обработки образцов. Энергия активации реакции окисления S02 на массивной платине и на платинированном силикагеле составляет 23 3 0 6 ккал / молъ. Каталитическая активность платинированного силикагеля на единицу веса платины остается приблизительно постоянной при изменении концентрации платины от 0 001 до 0 5 %; Следовательно, размеры кристаллов платины в платинированном силикагеле не зависят от концентрации платины и определяются только структурой пор силикагеля и предварительной тепловой обработкой. Каталитическая активность в реакции окисления S02 была определена для платины, вольфрама, золота, сплавов платина - золото, хрома, рубидия и серебра. Оказалось, что серебро каталитически неактивно. Все другие металлы, за исключением платины, имеют приблизительно одинаковую активность, однако меньшую, чем у платины. Херт [61] применил особый метод расчета для нахождения соотношения между данными по окислению S02 на платиновых катализаторах. [12]
Страницы: 1