Размер - молекула - растворитель
Cтраница 1
Размеры молекул растворителя также влияют на температуру плавления; понижение Гпл должно быть большим в растворителях с меньшим молярным объемом. [1]
Большое в размерах молекул растворителя и растворенного вещества заметно влияет на энтропийные характеристики раствора. Играют роль специфические черты длинных молекул, связанные с внутренними вращениями и выражающиеся в гибкости цепи, в наличии множества возможных конфигураций цепи. Теория растворов веществ предствляет собой относительно самостоятельную теории растворов. [2]
Если размеры сегмента равны размерам молекулы растворителя, то xN / ( n - - xN) равно относительной части объема, занимаемой полимером. [3]
Дипольный момент, поляризуемость, форма, размер молекул растворителя влияют на координационное число, длительность пребывания, прочность связи молекул реагентов в сиботаксических областях и тем самым и на условия образования активного комплекса. Сравнение поведения соединений, отличающихся главным образом на одну из молекулярных постоянных, позволяет вскрыть зависимость эффекта растворителя на скорость реакции от сил сцепления, формы, размера его молекул. [4]
В еще более концентрированных растворах важную роль играют размеры молекул растворителя и взаимодействия типа ион-растворитель. [5]
Слабым местом теории Ван-Лаара является допущение о равенстве размеров молекул растворителя и растворенного вещества. [6]
В мембране существуют поры, размеры которых больше размеров молекул растворителя, но меньше размеров молекул растворенного вещества. Поэтому через мембрану проходят только молекулы растворителя. Размеры латексных частиц 7000 - 10 000 нм больше размеров пор полимерных мембран ( 2000 - 3000 нм), поэтому латексные частицы полностью задерживаются мембраной. [7]
Полупроницаемая мембрана - перегородка, пропускающая малые по размеру молекулы растворителя, но не пропускающая крупные молекулы растворенного вещества. Перенос растворителя через мембрану обусловлен различием химических потенциалов растворителя по обе сторокы мембраны и связан с осмотическим давлением. Оно равно избыточному внешнему давлению, которое следует приложить со стороны раствора, чтобы прекратить осмос. В этом случае создаются условия осмотического равновесия - динамического равновесия, при котором скорости диффузии в прямом и обратном направлении равны. Превышение избыточного давления над осмотическим может привести к отрицательному осмосу - обратной диффузии растворителя. [8]
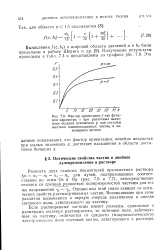 |
Фактор ориентации / как функция параметра а при различных значениях осевого отношения р для системы жестких эллипсоидальных частиц в ламинарном потоке. [9] |
Если растворенные частицы имеют размеры, сравнимые с размерами молекул растворителя, то истинное поле, действующее на частицу, отличается от среднего ( макроскопического) электрического поля световой волны, действующего в растворе. [10]
Ввиду малой подвижности макромолекул при растворении полимера небольшие по размеру молекулы растворителя легко проникают в пространство между звеньями полимерных цепей, раздвигая сначала их отдельные участки, а потом и сами цепи. Вследствие поглощения растворителя образец полимера увеличивается в массе и объеме. Этот процесс называется набуханием. Набухший полимер представляет собой раствор низкомолекулярной жидкости ( растворителя) в полимере. Перемещение ( диффузия) макромолекул в растворитель начинается тогда, когда цепи полимера уже достаточно раздвинуты и взаимодействие между ними ослаблено. [11]
Существуют веские основания считать толщину внутреннего слоя ( регулируемую размером молекул растворителя) фактором более важным, чем диэлектрическая проницаемость, когда речь идет об определении емкости и ее зависимости от потенциала в этих системах. [13]
В обычных условиях молекулы, размеры которых сравнимы с размерами молекул растворителя, будут распределены по всему объему пор геля. [14]
Отрицательные отклонения от идеальности обуславливаются действием двух факторов: различием размеров молекул растворителя и растворенного вещества ( так называемый атермический эффект) и наличием сильного взаимодействия между молекулами растворенного вещества и растворителя, которое превосходит взаимодействие между собой молекул растворенного вещества и молекул растворителя. В этом случае для растворенного вещества обычно значения у больше 1 и возрастают с увеличением концентрации. [15]
Страницы: 1 2 3 4
