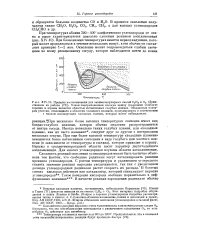
Размер - углеводородный радикал
Cтраница 2
Три простейших амина CH3NH2, ( CH3) 2NH, ( CH3) 3N, а также C2H5NH2, - газы с запахом аммиака, хорошо растворимые в воде. С увеличением размера углеводородных радикалов амины теряют запах аммиака и приобретают неприятный рыбный запах. Высшие амины - твердые вещества без запаха, не растворимые в воде. [16]
Водородные связи в спиртах слабее, чем в воде, но именно они обеспечивают довольно высокую температуру кипения и хорошую растворимость в воде. Водородные связи в первичных спиртах сильнее, чем во вторичных, которые, в свою очередь, образуют более сильные водородные связи, чем третичные. Сила образуемых водородных связей уменьшается также с увеличением размеров углеводородного радикала. [17]
Спирты, амины, карбоновые кислоты, амиды кислот способны растворяться в воде, так как они могут образовывать с водой водородные связи. При этом указанные соединения могут быть и донорами и акцепторами протонов, через которые связи осуществляются. Другие кислородные соединения - альдегиды, кетоны, простые и сложные эфиры - также могут образовывать с водой водородные связи, но они представляют собой только акцепторы протонов. Растворимость в воде определяется также размерами углеводородного радикала, связанного с активной группой - карбоксилом, аминогруппой или гидроксилом. При увеличении радикала растворимость в воде быстро падает. У высших спиртов или кислот остается только способность располагаться ориентированными молекулярными слоями на поверхности раздела вода - органический растворитель, причем активные группы, способные к образованию водородных связей, направлены к воде, а углеводородные радикалы к органическому растворителю. [18]
Дальнейшее обобщение вытекает из представлений о том, что защитное смещение электронов может передаваться ( 3-углеродному атому от несоседних атомов, хотя и со значительно меньшей интенсивностью. Так, защитный эффект, наблюдаемый в случае к-пропильной группы, увеличивается для к-бутильной группы, но в меньшей степени, чем для изобутильной. Как правило, в гомологическом ряду защитный эффект увеличивается до определенного предела, но при условии, что радикал с разветвленной цепью всегда оказывает большее влияние, чем изомерный радикал с нормальной цепью. Можно ожидать, что электроноакцепторные заместители, если не принимать во внимание размеры углеводородных радикалов, способствуют элиминированию и влияние их особенно сильно, если они непосредственно связаны с - углеродным атомом. [19]
Однако еще до возникновения научной теории растворов было установлено эмпирическое ( опытное) правило: подобное растворяется в подобном. Напротив, вещества ионного строения ( щелочи, соли) или полярные вещества ( спирты, альдегиды, кислоты) лучше растворимы в полярных растворителях. Например, расплавленные соли и щелочи неограниченно смешиваются друг с другом, если только не вступают в химическое взаимодействие между собой. Любопытно отметить, что простейшие спирты СН3ОН, С2Н5ОН, С3Н7ОН прекрасно растворимы в воде, но по мере того, как увеличивается размер углеводородного радикала в спирте ( C - iHgOH, С5НцОН), их растворимость в воде и, наоборот, растворимость воды в них уменьшается. Высшие спирты вообще практически нерастворимы в воде. [20]
При несколько более высоких температурах свечение имеет вид бледно-голубого пламени, которое обычно медленно распространяется от центра сосуда. Иногда несколько таких голубых пламен, или холодных пламен, как их часто называют, следуют друг за другом с интервалами несколько секунд. При еще более высокой температуре холодные пламена заменяются более интенсивным свечением в виде голубого или желтого пламени ( в зависимости от температуры и состава), которое приводит к взрыву. Для многих углеводородов изучены области воспламенения. Сложность реакций окисления углеводородов может быть частично объяснена тем фактом, что свободные радикалы могут катализировать реакции крекинга углеводородов. С ростом температуры и удлинением углеродного скелета значение реакций пиролиза увеличивается, так как с увеличением размера углеводородных радикалов растет скорость их распада. [22]
Страницы: 1 2