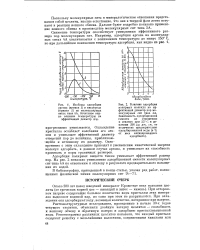
Эффективный размер
Cтраница 3
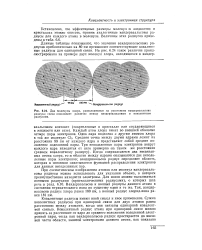 |
Две молекулы хлора, расположенные на расстоянии вандерваальсова радиуса. схема показывает различие между вандерваальсовым и ковалентным радиусами. [31] |
Установлено, что эффективные размеры молекул IB жидкостях и кристаллах можно описать, приняв аналогичные вандерваальсовы радиусы для каждого атома в молекуле. [32]
Здесь L - эффективный размер теплового пятна; г, z - цилиндрические координаты; ось z - направлена по вектору скорости набегающего потока. [33]
Таким образом, эффективный размер главного канала мордента регулируется введением катиона, обладающего соответствующим ионным радиусом. [34]
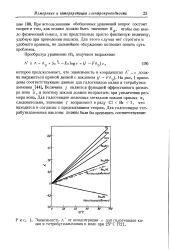 |
Зависимость л от концентрации с для галогенидов калия и тетрабутиламмония в воде при 25 С. [35] |
Величина является функцией эффективного размера иона а, и поэтому наклон должен возрастать при увеличении размера иона. Для галогенидов щелочных металлов наклон прямых и, следовательно, значение / возрастают в ряду С1 Вг I, что находится в согласии с предсказанием теории. [36]
Представляет интерес оценка эффективных размеров области, которую занимают электрон или дырка, связанные с соответствующими примесными, центрами. Для оценки может служить соответствующая величина радиуса боровской орбиты ап. [37]
А-фазе образуются поры, эффективный размер которых одинаков; газовая фаза состоит из т газообразных продуктов реакций, протекающих на стенках и внутри пор; скорость усадки материала покрытия мала по сравнению с линейной скоростью термохимического и механического разрушений; истинная плотность конденсированных компонентов постоянна; число выходов пор на единичную площадь границы раздела сред постоянно, действие объемных сил не учитывается; реакция разложения является реакцией первого порядка и следует закону Аррениуса с эффективным значением энергии активации. [38]
При адсорбции веществ, эффективные размеры молекул которых соизмеримы со входами в микропоры активного угля ( третичный бутил-бензол, 1 3 5-триэтилбензол на АУ-3), наблюдается эффект молекулярно-ситового действия, приводящий к общему снижению адсорбционной способности адсорбента, а сам процесс адсорбции приобретает активированный характер. Динамическая активность существенно снижается за счет ухудшения кинетики адсорбции. [39]
Отсюда следует, что эффективные размеры ионов галогенов в водных растворах примерно одинаковы, тогда как эффективный размер перхлорат-иона значительно больше. Следовательно, если бы селективность анионитов зависела в первую очередь от электростатического взаимодействия с образованием ионных пар, ионы С1 -, Вг - и 1 - поглощались бы ионитом примерно одинаково и значительно сильнее, чем ион ClOj. Но это противоречит экспериментальным данным, изложенным в разделе II.2. Кроме того, в случае сильноосновных анионитов нельзя ожидать существенного образования электростатических ионных пар ( типа пар Бьеррума) между обычными анионами и большим триалкилбензиламмониевым ионом ионита. [40]
Отсюда следует, что эффективные размеры ионов галогенов в водных растворах примерно одинаковы, тогда как эффективный размер перхлорат-иона значительно больше. Но это противоречит экспериментальным данным, изложенным в разделе II.2. Кроме того, в случае сильноосновных анионитов нельзя ожидать существенного образования электростатических ионных пар ( типа пар Бьеррума) между обычными анионами и большим триалкилбензиламмониевым ионом ионита. [41]
Снижение температуры способствует уменьшению эффективного размера пор молекулярных сит. [43]
Величина L носит название эффективного размера ОКР. [44]
Изученные явления требуют учета эффективного размера молекул при выборе рациональных адсорбентов, причем в ряде случаев невозможно проводить расчеты адсорбционных процессов с использованием констант, определенных по бензолу. [45]
Страницы: 1 2 3 4 5