Малый размер - катион
Cтраница 1
Малый размер катионов позволяет им хорошо внедриться в кварцеподоб-ную структуру высокосиликатной фазы, и она закристаллизовывается при низкой температуре с образованием кварцеподобных твердых растворов. Ситаллы этих систем обладают высокой степенью закристаллизо-ванности. Напротив, в ситаллах системы Si02 - А1203 - СаО - ТЮ2 высокосиликатная фаза обладает малой склонностью к кристаллизации, и ситаллы этой системы отличаются меньшей степенью закристаллизован-ности. Для этой и других систем с большими катионами ( Ва2, Na) склонность к кристаллизации высококатионной стеклофазы является единственным фактором, способным зафиксировать ( затормозить) развитие ликвационных процессов на нужном этапе. [1]
 |
Относительное расположение ионов металла. [2] |
Связь с ионами образуется большей частью в результате ионо-дипольного взаимодействия, причем образованию связи благоприятствует малый размер катиона, большой заряд его, например А13, и связанная с этим большая его поляризующая способность. При большом размере аниона с увеличением общего размера катиона ( вместе со связываемыми им молекулами воды) возрастает координационное число и при этом увеличивается устойчивость такой структуры. [3]
Когда легирующий элемент характеризуется неравенством UMeS UFeS, решеткой Me S, отличной от FeS, и имеет малые размеры катионов, то можно ожидать более быстрой диффузии последних по сравнению с ионами железа. [4]
Связь с ионами образуется большей частью с помощью донор-но-акцепторной связи или в результате ионо-дипольного взаимодействия, причем образованию связи благоприятствует малый размер катиона, большой заряд его, например А13, и связанная с этим большая его поляризующая способность. При большом размере аниона с увеличением общего размера катиона ( вместе со связываемыми им молекулами воды) возрастает координационное число и при этом увеличивается устойчивость такой структуры. [5]
Связь с ионами образуется большей частью с помощью до-норно-акцепторной связи или в результате ион-дипольного взаимодействия, причем образованию связи благоприятствует малый размер катиона, большой заряд его, например А13, и связанная с этим большая его поляризующая способность. При большом размере аниона с увеличением общего размера катиона ( вместе со связываемыми им молекулами воды) возрастает координационное число и при этом увеличивается устойчивость такой структуры. [6]
Связь с ионами образуется большей частью с помощью донор-но-акцепторной связи или в результате ионо-дипольного взаимодействия, причем образованию связи благоприятствует малый размер катиона, большой заряд его, например А13, и связанная с этим большая его поляризующая способность. [7]
Связь с ионами образуется большей частью с помощью донор но-акцепторной связи или в результате ионо-дипольного взаимо действия, причем образованию связи благоприятствует малый размер катиона, большой заряд его, например А13, и связанная с этим большая его поляризующая способность. При большом размере аниона с увеличением общего размера катиона ( вместе со связываемыми им молекулами воды) возрастает координационное число и при этом увеличивается устойчивость такой структуры. [8]
Малый заряд, а также ( хотя и в меньшей степени) большой размер катиона металла благоприятствуют предпочтительному образованию гидроокиси, а не окисла, в то время как высокая валентность и малый размер катиона благоприятствуют образованию истинного окисла. Например, окислы одновалентных щелочных металлов ( лития, натрия, калия) менее устойчивы, чем их гидроокиси, тогда как в случае четырехвалентных металлов ( например, титана и циркония) справедливо обратное: действительно, их гидроокиси неизвестны. Магний обычно образует гидроокись ( бруцит Mg ( OH) 2), в то время как алюминий в зависимости от температуры и состава раствора образует либо байерит ( ] 3-тригидрат А1 ( ОН) 3), либо бсмит ( а-моногидрат АЮ ( ОН)), либо истинную окись ( А12О3); железо ведет себя подобно алюминию. [9]
Бор является весьма своеобразным элементом как в отношении геохимических, так и химических свойств. Благодаря малым размерам катиона и высокому заряду бор проявляет большую склонность к ассоциации и к образованию изо - и гетерополикислот. Хорошая растворимость и летучесть многих борных соединений делает этот элемент легко подвижным и соответственно весьма рассеянным. По данным академика А. П. Виноградова [1], содержание бора в различных породах составляет - 10 - 3 вес. Огромные количества бора, содержащиеся в природных водах, делают их перспективными в качестве источников борного сырья. Особенно эффективным может быть метод селективного извлечения бора на ионитах и комплексо-образующих сорбентах. Рассмотрению возможностей извлечения бора из природных и технических вод и посвящена настоящая работа. [10]
Во фторидах натрия и лития гидратации катиона, препятствует малый размер аниона фтора. С другой стороны, малые размеры катионов лития и натрия препятствуют присоединению молекул воды анионом фтора за счет водородных связей. [11]
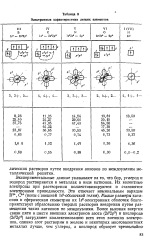 |
Электронные характеристики легких элементов. [12] |
Экспериментальные данные указывают на то, что бор, углерод и водород растворяются в металлах в виде катионов. Их валентные-электроны при растворении коллективизируются и становятся электронами проводимости. Малые размеры катионов и сферическая симметрия их 1 2-электронных оболочек благоприятствует образованию твердых растворов внедрения путем размещения таких катионов по междоузлиям. [13]
Среди специфических адсорбентов II типа с кислотными центрами на поверхности ( протонного и апротон-ного типа) или с катионированными поверхностями большой интерес представляют пористые кристаллы цеолитов. При не очень больших заполнениях зависимость адсорбции от концентрации в газе и от температуры описывается, как и на непористых поверхностях, уравнениями, приближенно учитывающими взаимодействие адсор-бат-адсорбат. Для молекул А меньших размеров, в том числе для низших алканов при более низких температурах, взаимодействия адсорбат-адсорбат приводят к перегибу на изотермах адсорбции цеолитами, особенно при адсорбции цеолитом LiX, поверхность полостей которого, благодаря малым размерам катионов Li, размещающихся между атомами кислорода решетки цеолита, особенно однородна. Зависимость адсорбции от температуры в этом случае учитывается соответствующими зависимостями от температуры констант равновесия адсорбат - адсорбент и адсорбат-адсорбат. Адсорбция молекул В с небольшими и особенно со значительными ( СО2) квад-рупольными моментами требует учета уменьшения теплоты адсорбции с ростом заполнения цеолита. [14]
Предположить полное отсутствие диффузии азота и водорода в покрытии невозможно, следует считать ее малой. Адсорбция азота и водорода поверхностью покрытия безусловно существует, следовательно, возможен переход адсорбированных атомов с поверхности в объем при наличии соответствующих условий. Очевидно такой переход будет более вероятен при наличии в объеме покрытия соответствующих дефектов и вакансий. Как было показано, кислород диффундирует в покрытие значительно легче, чем азот и водород, хотя размер иона кислорода значительно больше, чем, например, иона - водорода. В данном случае, очевидно, имеет значение тот факт, что в покрытии создается повышенная концентрация кислородных вакансий за счет ухода части кислорода на окисление металла на границе покрытие - металл, и. Азот и водород в состав покрытия не входят и их взаимодействие с металлом в начальные стадии невозможно. Эти газы, естественно, какой-то собственной растворимостью в покрытии обладают, но она мала, так как известно, что стекло и керамика в обычном состоянии азот и водород не поглощают. В таком случае ионы азота и водорода могут внедряться в кислородные вакансии как в междуузлия, но это внедрение, как показывает опыт, мало. Водород в силу малого размера катиона более подвижен, что и показывает опыт. [15]
Страницы: 1