Экстраполированная величина
Cтраница 2
Параметр восстановления Q определяет степень релаксации угловой скорости к ее экстраполированной величине: если Q 1, то Й ( 0 - Й0 ( 0 при t - оо. В данном случае Й0 ( 0 00 - at / I - это частота пульсара в отсутствие сбоя и П0 - постоянная. [16]
Первоначальное отношение изомеров 1 2 - / 2 3 - ( экстраполированная величина) лежало между 0 5 и 1, но возрастало в ходе реакции. [17]
В ряду полиалкилметакрилатов [38] ( рис. 354) при низких давлениях экстраполированная величина удельной поверхности ( область экстраполяции) значительно меньше, чем в случае полиалкилакрилатов. Замещение водорода в главной цепи на метильную группу вызывает ограничения в ориентации; цепи становятся менее гибкими, что приводит к изотермам, характерным для более жестких полимеров. Возрастание длины боковой цепи в макромолекуле способствует увеличению поверхности пленки по крайней мере в области низких давлений. При этом величина поверхности, занимаемая мономерным звеном, возрастает от 14 5 А2 для полиметилметакрилата до 30 5 А2 для поли-октадецилметакрилата. [18]
Один из наиболее ранних методов [1884] состоит в экстраполяции линейного участка ионизационной кривой к нулевому значению ионного тока и использовании экстраполированной величины как потенциала ионизации. Этот метод предполагает линейную зависимость между ионным током и энергией электронов вплоть до порогового значения, а наблюдаемый хвост кривой объясняют энергетической неоднородностью электронного пучка. В настоящее, время этот метод используется редко. В отдельных случаях, когда прямолинейная область обозначена достаточно отчетливо, он дает результаты удовлетворительной точности, и при этих обстоятельствах он имеет преимущества по сравнению с другими методами благодаря меньшей субъективности. Однако во многих случаях линейный участок кривой не вырисовывается достаточно резко, и при этих условиях метод совершенно непригоден. Основной недостаток состоит в том, что зависимость тока от энергии используется в области значительно выше ионизационного потенциала, где ионы не могут находиться в своем наинизшем энергетическом состоянии. Получаемые результаты обычно превышают данные других методов, особенно в тех случаях, когда определяются потенциалы появления осколочных ионов, образующихся при сложных реакциях. Было найдено [1872], что кривая для гелия значительно круче по сравнению с кривой для водорода: ионизационная кривая Не приближается к прямой, тогда как кривая Н обладает значительным изгибом. [19]
Данные о том, что кремниевая кислота обладает более высокой растворимостью, чем кварц, получены сравнением данных Кеннеди с экстраполированными величинами Штрауба, измерившего растворимость кремниевой кислоты в перегретом паре. [20]
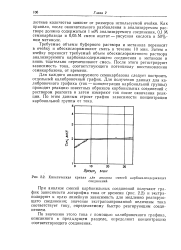 |
Кинетическая кривая для анализа. [21] |
При анализе смесей карбонильных соединений получают график зависимости логарифма тока от времени ( рис. 2.2) и экстраполируют к нулю линейную зависимость для медленно реагирующего соединения; значение экстраполированной величины тока соответствует току, определяемому быстро реагирующим соединением. [22]
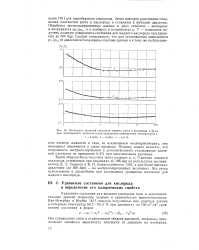 |
Отношение значений плотности жидких азота и кислорода в функции приведенного давления и при одинаковых приведенных температурах т. [23] |
Таким образом была получена сетка опорных р, v, Г - данных жидкого кислорода, основанная при давлениях до 196 бар на результатах экспериментов Д. Л. Тимрота и В. П. Борисоглебского [39], а при более высоких давлениях ( до 500 бар) - на экстраполированных величинах. Эта сетка использована в дальнейшем при составлении уравнения состояния для жидкого кислорода. [24]
В графах 4 и 5 показаны стандартные ошибки для концентраций примесей на уровне 10 - 8 - 10 - 9 г. Для ряда элементов ( Mg, Fe, A1, Си), некоторые количества которых находились в контрольной пробе ( электрод, вода и носитель), в скобках приведены экстраполированные величины чувствительности. [25]
Экстраполированная величина G ( O2) при нулевом давлении [ g ( O2) ] равна 0 33 и находится в хорошем согласии с теоретическим выходом, установленным для этого реактора. Это отчасти не согласуется с утверждением Хэммера и др. [17], цитированным ранее, что эффективность выделения газа близка к эффективности, соответствующей равновесному распределению. [26]
Холостой опыт проводят параллельно с основным определением, заменяя анализируемую порцию 50 см3 воды. Если величина абсорбции холостого определения существенно отличается от экстраполированной величины абсорбции нулевого члена ( см, построение градуировочного графика), то следует найти причины различия. [27]
Тиммерманс [1501] приводит значение Тт для фенола, равное 313 90 К; Бидискомб и Мартин [129] измерили давление пара жидкого и твердого фенола. Аитуана (1.12) к температуре плавления фенола приводит к занижению экстраполированных величин по сравнению с давлением пара, измеренным над твердым фенолом, на величину около 0 06 мм рт. ст. Введение небольшой поправки в коэффициент уравнения Антуана приводит к совпадению давлений паров твердого и жидкого фенола в тройной точке. [28]
Холостой опыт проводят параллельно с основным определением, заменяя анализируемую порцию 50 мл воды. Если поглощающая способность при холостом определении существенно отличается от экстраполированной величины поглощения нулевого члена ( см. построение гра-дуировочного графика), то следует найти причины различия. [29]
Тиммерманс [1501] приводит значение Тт для фенола, равное 313 90 К; Бидискомб и Мартин [129] измерили давление пара жидкого и твердого фенола. Поскольку давление пара жидкого фенола определяли в интервале температур 394 - 455 К, экстраполяция полученного авторами [129] уравнения Антуана (1.12) к температуре плавления фенола приводит к занижению экстраполированных величин по сравнению с давлением пара, измеренным над твердым фенолом, на величину около 0 06 мм рт. ст. Введение небольшой поправки в коэффициент уравнения Антуана приводит к совпадению давлений паров твердого и жидкого фенола в тройной точке. [30]
Страницы: 1 2 3