Разность - потенциал - металл
Cтраница 1
Разность потенциалов металла и окислителя определяют возможность коррозии. Более важной характеристикой служит скорость коррозии, выражаемая через потери металла в единицу времени. Скорость коррозии может быть также выражена по закону Фарадея через ток или плотность тока. [1]
Разность потенциалов металла и окислителя определяет возможность коррозии. Более важной характеристикой служит скорость коррозии, выражаемая через потери металла в единицу времени. Скорость коррозии может быть также выражена по закону Фарадея через силу тока или через плотность тока. [2]
Разность потенциалов металла и окислителя определяет возможность коррозии. Более важной характеристикой служит скорость коррозии, выражаемая через потери металла в единицу времени. Скорость коррозии может быть также выражена по закону Фарадея через ток или плотность тока. [3]
Скорость разрушения покрытия зависит от разности потенциалов контактирующих металлов. Чем эта разность больше, тем быстрее протекает разрушение. [4]
Величина тока в гальванической ( контактной) паре зависит ст разности потенциалов металлов, а также от омического ео-нрогивления коррозионной среды и поляризации электродов в процессе работы пары. [5]
Своеобразным методом серебрения является электролиз без внешнего источника тока, за счет разности потенциалов металла покрываемых деталей и цинковой пластинки, так называемое серебрение с корабликом. Сущность его заключается в том, что на поверхности электролита помещается свободно плавающая деревянная коробочка с дном в виде диафрагмы из бычьего пузыря, наполненная концентрированным раствором поваренной соли. В коробочку укладывается пластинка цинка, соединенная гибким проводником с изделием, помещенным в цианистый электролит серебрения. Этот метод контактного серебрения, при известной модернизации, может быть использован в случае отсутствия источников тока для серебрения изделий с небольшой толщиной покрытия. [6]
При наложении цинкового покрытия не требуется создания совершенной непроницаемости покрытия, так как электролит, проникая в поры слоя, создает гальванические пары, потенциал которых определяется разностью потенциалов металлов, образующих эти пары. Так как железо имеет более положительный потенциал, чем цинк, в результате воздействия электролита начинается разрушение цинка; железо при этом не разрушается. [7]
Интенсивность коррозии зависит от разности потенциалов соприкасающихся металлов и от электропроводности окружающей их жидкости. Чем больше разность потенциалов металлов и электропровод-ость жидкости, тем интенсивнее проявляется коррозия. [8]
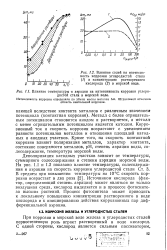 |
Влияние температуры и аэрации на интенсивность коррозии углеродистой стали в морской воде. [9] |
Металл с более отрицательным потенциалом становится анодом и растворяется, а металл с менее отрицательным потенциалом является катодом. Коррозионный ток и скорость коррозии возрастают с увеличением разности потенциалов металлов и отношения площадей катодных и анодных участков. Кроме того, на скорость контактной коррозии влияют поляризация металлов, характер контакта, состояние поверхности металлов, рН, степень аэрации воды, со-лесодержание, температура морской воды. [10]
Металл с более отрицательным потенциалом ( анод) в этом случае начнет разрушаться со скоростью, значительно превышающей ско - % рость коррозии этого металла и отсутствие контакта. Разность потенциалов контактирующих металлов не определяет однозначно скорость их коррозии, которая зависит от силы тока в системе, контролируемой в большинстве случаев поляризационными явлениями. [11]
Детали запружаются В: раствор иод током. Величина катодного тока должна быть достаточной для смещения потенциала металла-подложки в отрицательную сторону настолько, чтобы исключалась возможность его анодного растворения. Такой метод дает хорошие результаты, если разность потенциалов металлов невелика ( например, в некоторых комплексных электролитах), а поляризация при осаждении электроположительного металла значительна. [12]
В контактной паре свинцовая оболочка - стальная броня в зависимости от состава окружающей среды свинец может быть как катодом, так и анодом. Так, свинцовая оболочка в контакте со стальной броней является анодом в щелочных средах, в торфяном и песчаном грунте. Ток, обусловленный действием этой пары, будет зависеть от разности потенциалов металлов, электрического сопротивления элементов цепи и поляризации электродов, возникающей при протекании тока. При этом возможна коррозия оболочки даже при отсутствии коррозии брони. [13]
На содовых заводах хлористый аммоний получают высаливаем его вз фильтровой жидкости, насыщенной аммиаком и углекислотой, о помощью поваренной соли. Высаливание хлористого аммония осуцествляется в кристаллизаторах, трубы которых охлаждаются хладагентом ( раствором t / a tlt Со. В теплообменниках кристаллизаторов в контакте о чугуном в углеродистой сталью работает нержавеиая сталь, что приводит х интенсивной коррозии этого матервала, являющегося анодов гальванического элемента. Скорость коррозии зависит от разности потенциалов металлов, соотношения площадей анода и катода и электропроводности среды. [14]
Страницы: 1