Разность - энергия - орбиталь
Cтраница 1
 |
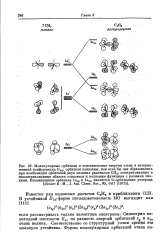
Влияние я-связи на энергетический уровень T2g и. [1] |
Разность энергий орбиталей T2g и Ее составляет QDq. С возрастанием прочности а-связи металл-лиганд орбитали Eg понижаются, a Eg повышаются на такую же величину и Dq возрастает. Если электроны металла на орбиталях T2g образуют л-связи с пустыми р - или d - орби-талями лигандов, энергия уровня T2g в комплексе понижается и Dq возрастает. [2]
Если разность энергий орбиталей центрального иона комплекса и лигандов будет очень велика, то энергия стабилизации за счет образования молекулярных орбиталей может быть не очень высокой. В тоже время в ряде случаев между центральным ионом и лигандами действует сильное электростатическое притяжение. Таким образом, координационная связь в комплексах может иметь различный характер, изменяясь от чисто ионной до ионной с большим вкладом ковалентной составляющей ( гл. [3]
Симметрия переходной плотности Еи, но разность энергий орбиталей eg и а2ц очень велика. Соответственно со структурной точки зрения эта молекула устойчива. [5]
 |
Отнесение электронных возбужденных состояний в фторидах ксенона. [6] |
Теоретическое значение энергии перехода приближенно определяется разностью энергий орбиталей. [7]
Если мы непосредственно рассчитаем энергии возбужденных состояний, то обнаружим, что разности энергий орбиталей не равны энергии возбуждения и что необходимо явно учесть изменение в отталкивании электронов в основном и возбужденном состояниях. Это означает, что возбуждение с ВЗМО на HGMO не обязательно приводит к низшему по энергии возбуждению. [8]
Тот факт, что многие внутрийомплексные соединения Fe2 с сильными электронодонорными лигандами имеют зеленый цвет, свидетельствует о малой чувствительности полос ПЗ в спектрах комплексов к изменению электронодонорности ли-гандов. По-видимому, уровни энергии верхних занятых МО лигандов и вакантных АО центрального иона металла таковы, что разности энергий орбиталей, между которыми осуществляются электронные переходы, остаются приблизительно одинаковыми: малая донорность лиганда компенсируется большей акцепторностью центрального иона, и наоборот. То же по-видимому, относится и к разности энергий d - электронов металла и л - МО лиганда, между которыми происходят d - я - переходы, также ответственные за поглощение света в длинноволновой области. [9]
Это дает p0ft симметрии ng X яи 2 или Аи. Наиболее легким молекулярным процессом должна быть диссоциация на СО О или, возможно, искажение до структуры с неравными длинами связей. Разность энергий орбиталей ng и я велика, и молекула устойчива в линейной симметричной конфигурации. [11]
По этой причине 30е - орбиталь рассматривалась как связывающая, а 4ай - орбиталь как разрыхляющая. В действительности, конечно, все три орбитали смешиваются, причем отношение коэффициентов перед ними в орбиталях 30g, 4ag PI 50g зависит от разностей энергий орбиталей 2sx, 2sy и 2ру Для молекулы СО2, согласно Маллигану [887] и Малликену [892, 914], коэффициент перед 2 с-орбиталью в орбитали 30g относительно мал, в силу чего орбиталь 30g будет несвязывающей. [12]
Диссоциативная адсорбция водорода изучена достаточно хорошо, что нельзя сказать об адсорбционных состояниях других молекул, тогда как, чтобы объяснить механизм каталитической реакции, необходимо в первую очередь представить структуру адсорбированного на активных центрах реагента или промежуточных продуктов реакции. Рассмотрим, например, адсорбцию моноксида углерода СО. Как показано на рис. 5.4, электроны высшей заполненной молекулярной ор-битали ( ВЗМО) 5а могут переходить на незаполненные уровни поверхности металла, а одновременно с заполненных уровней поверхности электроны переходят на 2чг - орбиталь молекулы СО. Изменение в разности энергий орбиталей 1тг и 4ст ( величина & Е17Г - Е4а) составляет 2 6 - 3 5 эВ в зависимости от вида адсорбирующего металла. [13]
Страницы: 1