Низкая величина - энергия - активация
Cтраница 1
Низкая величина энергии активации, порядка 2 - 15 ккал / молъ, указывает на зависимость характеристического показателя процесса от физических процессов, таких как диффузия, адсорбция и десорбция, испарение, возгонка и растворение. Высокие энергии активации указывают на то, что скорость процесса определяется химическими реакциями. В этом случае величина энергии активации составляет около половины энергии разрыва химической связи. [1]
Заметно низкие величины энергий активации, которые наблюдаются для реакции N0 - CJo и NO Bi 2, могут явиться результатом подобного сложного пред-равновесия. Отсюда следует необходимость дальнейшего тщательного изучения этих систем. Все остальные реакции, представленные в табл. XII.9. относятся к такому типу, в котором третье тело действует как переносчик избыточной энергии реакции ассоциации. Экспериментальные данные показывают, что эффективность различных третьих тел может быть различной. В случае 1 1 эффективность мезитилена вЗ раза больше, чем других больших молекул, и примерно в 100 раз больше, чем Не. Эти результаты качественно согласуются с ожидаемыми изменениями по мере увеличения сложности молекул ( разд. Оказывается, иод может образовать долгоживущие метастабильные частицы. [2]
Заметно низкие величины энергий активации, которые наблюдаются для реакций NO C12 и N0 Br2, могут явиться результатом подобного сложного пред-равновесия. Можно видеть, что для рекомбинации атомов Вг и I частотные-факторы находятся в пределах ожидаемого порядка величины, а именно 1010л2молъ - 2 сек1, а энергии активации, по-видимому, равны нулю. Экспериментальные данные показывают, что эффективность различных третьих тол может быть различной. В случае I I эффективность мезитилена в 3 раза больше, чем других больших молекул, и примерное 100 раз больше, чем Не. Эти результаты качественно согласуются с ожидаемыми изменениями но мере увеличения сложности молекул ( разд. Оказывается, иод может образовать долгоживущие метастабильные частицы. [3]
Низкая величина энергии активации процесса деструкции ( 20 - - 70 ккал / моль) по сравнению с энергией связи Si-О ( 101 - - 118 ккал / моль, см. табл. 2), по-видимому, обусловливается облегчением расщепления силоксановой связи в результате образования переходного комплекса. [4]
Для всех рассматриваемых углеводородов характерны низкие величины энергии активации, лежащие в пределах 20 000 - 26 000 жал. [5]
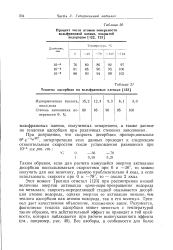 |
Теплоты адсорбции на вольфрамовых пленках. [6] |
Этот момент Трепнел отметил [123] при рассмотрении низкой величины энергии активации op / no-napa - превращения водорода на металлах; скорость-определяющей стадией оказывается десорбция атомов водорода, однако энергия ее активации меньше, чем теплота адсорбции как атомов водорода, так и его молекул. Трепнел дает качественное объяснение, изложенное выше. [7]
Для оценки реакционной способности частиц в молекулярных и радикальных реакциях, протекающих при низких величинах энергий активации, особенно большое значение приобретает знание стерических факторов. Чаще это можно ожидать именно при радикальных реакциях. Поэтому большое значение приобретает разработка доступного метода вычисления и надежных экспериментальных способов определения величин стерических факторов радикальных реакций. [8]
Что касается первой возможности, то прямые экспериментальные доказательства о распределении поверхностей, характеризующихся низкими величинами энергии активации, будет получить очень трудно. [9]
Отсутствие члена с хг свидетельствует о том, что в выбранных пределах варьирования переменных температура заметной роли не играет и может служить указанием на низкую величину энергии активации процесса этинилирования. Поскольку в рассматриваемой системе существенный вес имеют парные взаимодействия, степень влияния каждого из факторов следует оценивать по так называемым частным эффектам. [10]
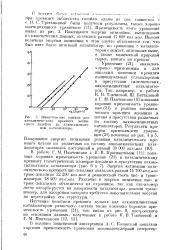 |
Кинетические кривые для каталитического крекинга эмбин. [11] |
Кажущаяся энергия активации, вычисленная из кинетических данных, оказалась равной 17 600 кал мол. Низкая величина энергии активации в этом случае объясняется тем, что был взят более активный катализатор, по сравнению с катализатором в опытах, описанных выше, а также химической природой сырья, взятого на крекинг. [12]
По-видимому, весьма вероятно, что большинство активных центров в молекулах ферментов имеет больше чем одну группу, способную образовать связь с частями субстрата. Низкие величины энергии активации могут являться результатом одновременной атаки несколькими группами, весьма схожей с пуш-пул механизмами, предложенными для реакций гидролиза, катализируемых кислотами и основаниями. Было найдено, что наличие и кислотной, и основной групп в соответствующих положениях в одной молекуле может быть намного эффективнее, чем наличие тех же групп, но в раздельных молекулах. Возможно, что в реакциях окисления и восстановления от субстрата к ферменту и наоборот переносятся не ионы, а радикалы. И в этом случае более благоприятным с энергетической точки зрения может быть одновременный перенос к соседним местам и от них, чем определенная последовательность в разрыве и образовании связей. Целесообразно провести сравнение с механизмом Ридила в гетерогенно-каталитических реакциях гидрирования, где один атом водорода удаляется с поверхности, в то время как другой атом из газовой фазы садится на соседнее место. [13]
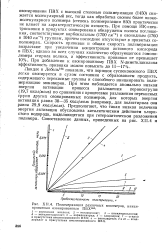 |
Полимеризация различных мономеров, инициированная озонированным ПВХ164. [14] |
Ландле и Лебедь164 показали, что порошок суспензионного ПВХ легко озонируется в сухом состоянии с образованием продукта, содержащего перекисные группы и способного инициировать полимеризацию мономеров. Предполагают, что такая низкая величина энергии активации обусловлена каталитическим действием хлористого водорода, выделяющегося при гетеролитическом разложении полимера. [15]
Страницы: 1 2