Разработка - электрод
Cтраница 2
Таким образом, электроды сравнения из металлов хотя и обладают рядом достоинств, однако, методика их приготовления сложна, так как электрохимическое поведение металлов зависит от состояния поверхности электрода. Этот фактор ограничивает срок службы таких электродов сравнения. В связи с этим значительное внимание было уделено разработке электродов сравнения типа электродов второго рода. Соли металлов несравненно менее чувствительны к загрязнениям как из атмосферы, так и из раствора по сравнению с самими металлами, поэтому электроды второго рода обладают обычно более стабильным потенциалом во времени. [16]
Исследование зависимости скорости внедрения щелочного металла от структуры электрода привело Кабанова, Киселеву, Астахова и Томашову [195] к выводу о важной роли вакансий в решетке металла в процессе внедрения. Согласно данным работы [195], с ростом числа вакансий в решетке металла у поверхности скорость внедрения возрастает. Именно с этим связано ускоряющее влияние на внедрение щелочного металла так называемой разработки электрода [203], то есть последовательности продолжительной катодной, анодной и вновь катодной поляризации. [17]
Развитие ручной дуговой сварки, на долю которой до сих пор приходится еще значительный объем ( 50 %) сварочных работ, стало возможным благодаря разработке электродов со специальными покрытиями, обеспечивающими получение высококачественного сварного шва. [18]
Однако пользоваться им для производственных измерений неудобно, поэтому рН - метры с водородными электродами применяются только как лабораторные приборы. Для производственных измерений используются индикаторные электроды из некоторых других веществ, обнаруживших свойства, аналогичные свойствам водородных электродов: хингидронные, сурьмяные и стеклянные. Первый из перечисленных электродов широко применялся на первых стадиях развития рН - метрии, однако пользоваться им, особенно для производственных измерений, также неудобно, поэтому с разработкой более совершенных электродов ( сурьмяных и особенно стеклянных) он почти совершенно вышел из употребления. [19]
Йсследова ние анодных материалов показало, что системы ( CeO2) o e ( La2O3) o 4 и ( СеО2) о в ( У2Оз) о 4 могут быть использованы в качестве анода ТЭ. В элементе с такими анодами удается получить плотность тока 0 1 А / см2 при напряжении 0 7 В. Разработка недорогих электродов и технология получения тонких электролитов открывает широкие перспективы развития ТЭ с твердыми электролитами. [20]
Таким образом, стандартный окислительный потенциал системы ион металла - металл может быть найден с помощью гальванического элемента без жидкостного соединения, полуэлементы которого обратимы к ионам соли металла. По-видимому, слабое ком-плексообразование между ионами соли не будет влиять на точность определения стандартного окислительного потенциала, поскольку оно учитывается средним коэффициентом активности. Применение гальванических элементов без жидкостного соединения для рассматриваемых целей ограничено небольшим набором электродов, обратимых к ионам металла. Успехи в области разработки ионселек-тивных электродов [105], включая стеклянные электроды с металлическими функциями [107], создают новые возможности в этом отношении. Представляет интерес электрод, обратимый к ионам ClOi [146], в силу слабой, в общем случае, склонности этого аниона к образованию комплексов. [21]
Эти электроды обладают широкими пределами выполнения функций соответствующих анионов с угловыми коэффициентами, близкими к теоретическому, высокой селективностью в присутствии ряда посторонних ионов, малым временем отклика. Величины их потенциалов в серии электродов одного типа близки друг к другу и хорошо воспроизводятся во времени. Вместе с тем наличие в этих электродах внутреннего водного раствора приводит к определенным трудностям при транспортировке и хранении электродов, а также в ряде случаев делает такие электроды неудобными в эксплуатации. Кроме того, наличие внутреннего водного раствора становится крайне нежелательным при разработке миниатюрных электродов для медико-биологических исследований. [22]
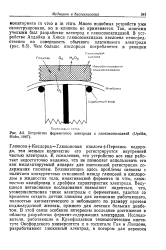 |
Устройство ферментного электрода с глюкозооксидазой ( Updike Hicks, 1967. [23] |
Глюкоза КислородГлкжоновая кислота Перекись водорода, тем меньше количество его регистрируется внутренней частью электрода. К сожалению, это устройство все еще работает недостаточно надежно, что не позволяет использовать его как имплантируемый аппарат для постоянной регистрации содержания глюкозы. Возникающие здесь проблемы связаны с наличием конкурентных отношений между глюкозой и кислородом в жидкостях тела, инактивацией фермента in vivo, сложностью калибровки и дрейфом характеристик электрода. Ведущиеся интенсивные исследования позволяют надеяться, что, усовершенствовав такие электроды с ферментами, удастся со временем создать датчик глюкозы для автономно работающего, полностью автоматического и небольшого по размеру протеза поджелудочной железы, нужного для лечения больных диабетом. В этой связи особенно интересны последние достижения в области разработки фермент-содержащих электродов. [24]
Совершенно иначе обстоит дело с разработкой совершенных силовых установок топливных элементов, которые должны отвечать ряду требований; обладать строго определенной характеристикой, достаточным сроком службы, приемлемым размером, надежностью в работе и быть экономичными. Разработка системы водородно-кислородного топливного элемента достигла такой стадии, когда следует обратить внимание на выполнение этих требований. В результате сейчас осуществляется обширная программа по разработке силовых установок и вводятся в действие совершенные силовые системы. Полупромышленная модель силовой установки на 2 кет показана на фиг. Чтобы поддержать усилие, направленное на создание этой силовой системы, особое внимание было обращено на разработку электродов и методов их изготовления, позволяющих получать прочные и воспроизводимые структуры с большим сроком службы и устойчиво улучшенную характеристику. [25]
Страницы: 1 2