Частичный разрыв - водородная связь
Cтраница 1
Частичный разрыв водородных связей приводит к тому, что различные молекулы воды находятся в разных состояниях. [1]
Денатурация ДНК - полный или частичный разрыв водородных связей между парами азотистых оснований, ведущий к раскручиванию полинуклеотид-ных цепей ДНК и их последующему разделению. Процесс денатурации обычно осуществляют путем нагревания растворов ДНК или же обработкой химическими реагентами. Жесткая двойная спираль ДНК после полной денатурации дает две значительно более гибкие молекулы, быстро свертывающиеся в беспорядочные клубки. Температуру, при которой отмечается середина структурного перехода спираль - клубок, называют т емпературой плавления. Ее рассматривают как температуру фазового перехода. Этот переход сопровождается изменениями всех основных молекулярных параметров ДНК. [2]
Большая часть ее расходуется на указанный частичный разрыв водородных связей между молекулами воды в кристаллах льда. [3]
Вторичная структура и ДНК, и РНК в значительной степени определяется водородными связями между парами комплементарных азотистых оснований, поэтому любые воздействия, способные разрушать водородные связи, могут менять пространственную организацию нуклеиновых кислот. Полный или частичный разрыв водородных связей, ведущий к раскручиванию полинуклеотидных цепей нуклеиновой кислоты и их последующему разделению, называется денатурацией. Кроме того, такие соединения, как амиды ( формамид, мочевина), увеличивая сольватацию ароматических ядер азотистых оснований молекулами воды, также способствуют разрыву водородных связей между основаниями. Денатурация нуклеиновых кислот может быть обратимым процессом; скорость ренатурации тем больше, чем меньше степень денатурации. Например, при полной денатурации ДНК нагреванием две комлементарные нити реассоци-ируют очень медленно ( происходит гак называемый отжиг ДНК) и только при медленном охлаждении раствора ДНК. При быстром охлаждении степень ренатурации невелика. [4]
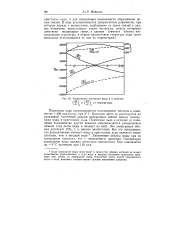 |
Зависимость плотности воды d и величин dd. ( dV. [5] |
Плавление льда сопровождается поглощением теплоты в количестве 1 436 ккал / моль при 0 С. Большая часть ее расходуется на указанный частичный разрыв водородных связей между молекулами воды в кристаллах льда. Увеличение объема воды при ее замерзании означает, что с повышением давления температура замерзания воды должна несколько понижаться. [6]
Плавление льда сопровождается поглощением теплоты в количестве 1 436 ккал / моль при 0 С. Большая часть ее расходуется на указанный частичный разрыв водородных связей между молекулами воды в кристаллах льда. Увеличение объема воды при ее замерзании означает, что с повышением давления температура замерзания воды должна несколько понижаться. Она понижается до - 1 С примерно при 130 бар. [7]
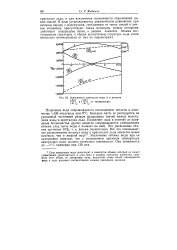 |
Зависимость плотности воды d и величин ldd ldV ( W p (. IT, Т темпеРатУРЫ. [8] |
Плавление льда сопровождается поглощением теплоты в количестве 1 436 ккал / моль при 0 С. Большая часть ее расходуется на указанный частичный разрыв водородных связей между молеку - 1ами воды в кристаллах льда. Увеличение объема воды при ее замерзании означает, что с повышением давления температура замерзания воды должна несколько понижаться. [9]
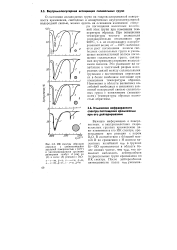 |
ИК спектры образцов аэросила с уменьшающейся удельной поверхностью 5 ( м2 / г и увеличивающимися средними размерами глобул d ( нм до ( / и после ( 2 реакции с D20. [10] |
С наблюдается рост поглощения полосы свободных силанольных групп и уменьшение низкочастотной полосы поглощения силанольных групп, связанных внутримолекулярными водород - ными связями. Это указывает на ослабление и частичный разрыв водородных связей между силанольными группами с постепенным переходом их в более свободное состояние при повышении температуры образца. Изменения в области валентных колебаний свободных и связанных взаимной-водородной связью силанольных групп с понижением ( повышением) температуры образца полностью обратимы. [11]
Рассмотренные эффекты не исчезают мгновенно после прекращения действия магнитного поля. Вода некоторое ( и довольно значительное) время сохраняет измененные свойства ( а следовательно, и строение) и лишь постепенно переходит в нормальное состояние. Это показывает, что такие процессы обладают релаксационным характером, по-видимому, из-за того, что перестройка относительного расположения молекул требует частичного разрыва водородных связей между молекулами, и это тормозит процесс. В той или другой степени влияние произведенного воздействия сохраняется в течение нескольких минут и часов. [12]
Рассмотренные эффекты не исчезают мгновенно после прекращения действия магнитного поля. Вода некоторое ( и довольно значительное) время сохраняет измененные свойства ( а следовательно, и строение) и лишь постепенно переходит в нормальное состояние. Это показывает, что такие процессы обладают релаксационным характером, по-видимому, из-за того, что перестройка относительного расположения молекул требует частичного разрыва водородных связей между молекулами, и это тормозит процесс. В той или другой степени влияние произведенного воздействия сохраняется в течение нескольких минут и часов. Высокой чувствительностью к различию внутреннего строения воды обладают некоторые биологические процессы. [13]
Подобные отклонения можно наблюдать и для результатов, полученных в других растворителях, что, очевидно, объясняется применением упрощающих предположений. Одним из таких предположений является допущение, что вклад вращения и колебания в частные функции в активном и в основном состояниях одинаков. Наоборот, жидкости, не обладающие упорядоченной структурой, вероятно, имеют в основном состоянии больше вращательных степеней свободы, чем в активированном. Этот эффект уменьшает вычисленное значение коэффициента диффузии. В растворителях, имеющих достаточно высокую степень упорядочения ( например, в воде), влияние вращательных степеней свободы при принятой методологии расчетов противоположно, и это приводит к тому, что вычисленные значения коэффициента диффузии ниже, чем измеренные. В воде и других, содержащих гидроксильные группы жидкостях молекулы связаны между собой водородными связями, простирающимися на расстояния, гораздо большие, чем молекулярные размеры. Из рассмотрения экспериментальных данных по вязкости можно заключить, что диффузия сопровождается некоторым разрушением внутренней структуры жидкости и частичным разрывом водородных связей в активном состоянии. Это уменьшает теоретически вычисленные значения коэффициента диффузии. В табл. 3.3 сопоставлены коэффициенты диффузии, вычисленные по уравнению (3.1.65) и установленные экспериментально в разбавленных водных растворах. [14]
Страницы: 1