Совместный разряд - катион
Cтраница 1
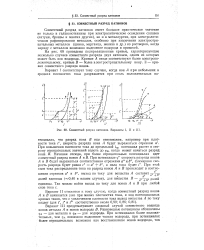 |
Совместный разряд катионов. Варианты I, II и III. [1] |
Совместный разряд катионов имеет большое практическое значение не только в гальванотехнике при электролитическом осаждении сплавов ( латуни, бронзы и многих других), но и в металлургии, при электролитическом рафинировании металлов, особенно при извлечении электроотрицательных металлов ( цинка, марганца, железа и др.) из растворов, когда наряду с металлом возможно выделение водорода и примесей. [2]
Совместный разряд катионов протекает в режиме химической и диффузионной кинетики. Это устанавливается на основании анализа общих и парциальных поляризационных кривых. [3]
Совместный разряд катионов двух различных металлов представляет собой одну из важнейших проблем электрохимии металлов. Это явление имеет место при электролитическом осаждении металла из раствора, содержащего примеси других металлов. [4]
Совместный разряд катионов Mz и Н3О ( или Н2О) становится возможным, если равновесный потенциал реакции (V.42) мЕр более отрицательный, чем равновесный потенциал реакции (V.43) н ер, или же если мер олее положительный, чем н2Ер, но металл выделяется с большим перенапряжением. [5]
Совместный разряд катионов Мг и Н3О ( или Н2О) становится возможным, если равновесный потенциал реакции (V.42) мбр более отрицательный, чем равновесный потенциал реакции (V.43) н вр, или же если мер олее положительный, чем нгер, но металл выделяется с большим перенапряжением. [6]
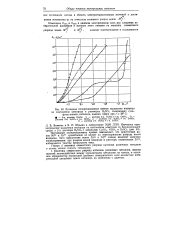 |
Катодные толшризапдоаные кривые выделения водорода на платиновом электроде в растворах H2SO4, содержащих сульфаты никеля, кобальта, кадмия, цинка при t 20 С. [7] |
Кинетика совместного разряда катионов различных металлов, помимо явлений взаимодействия между осаждаемыми металлами на катоде, в основном определяется структурой двойного электрического слоя вследствие избирательной адсорбции одних катионов, по сравнению с другими. [8]
Поляризационные кривые совместного разряда катионов на катоде для большинства процессов в широком интервале плотности тока получают при переменном химическом составе электролитического осадка. Вследствие этого равновесный ( если он может быть достигнут) или стационарный потенциал при изменении плотности тока не является величиной постоянной. Поэтому поляризация при осаждении сплава не может быть функцией одной переменной - плотности тока, а должна рассматриваться как функция нескольких переменных. [9]
Рассмотренные положения теории совместного разряда катионов могут быть весьма полезными для оценки влияния различного рода примесей на основной катодный процесс. Все примеси, сопутствующие разряду основного металла, делятся на две группы: примеси, потенциал выделения которых положительнее соответствующего потенциала для основного металла, и примеси электроотрицательные. Из возможных примесей к первой группе наиболее часто относятся благородные металлы, а также селен, теллур и др. Опыт показывает, что электроположительные примеси осаждаются IB условиях предельного для них тока при потенциале, соответствующем разряду ионов основного металла. [10]
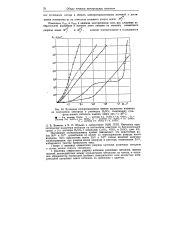 |
Катодные толшризапдоаные кривые выделения водорода на платиновом электроде в растворах H2SO4, содержащих сульфаты никеля, кобальта, кадмия, цинка при t 20 С. [11] |
Говоря о явлениях совместного разряда катионов различных металлов в целом, можно сказать следующее. [12]
Показано, что на кинетику совместного разряда катионов различных Металлов распространяются закономерности, вытекающие из теории замедленного разряда. [13]
Ml играет очень большую роль в кинетике совместного разряда катионов. [14]
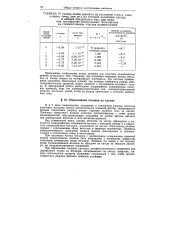 |
РАЗРЯД ионов КОБАЛЬТА из РАСТВОРОВ o. oooi - н. Cuso4. [15] |
Страницы: 1 2