Термодинамическая величина
Cтраница 1
Термодинамические величины, характеризующие вещество в его стандартном состоянии, называются стандартными величинами. Изменения термодинамических величин при реакции, в ходе которой исходные вещества в стандартном состоянии превращаются в продукты реакции, также находящиеся в стандартном состоянии, называются стандартными изменениями соответствующих величин. [1]
Термодинамические величины, характеризующие вещество в его стандартном состоянии, называются стандартными величн-н а м и. Изменения термодинамических величин при реакции, в ходе которой исходные вещества в стандартном состоянии превращаются в продукты реакции, также находящиеся в стандартном состоянии, называются стандартными изменениями соответствующих величин. [2]
Термодинамические величины, характеризующие вещество в его стандартном состоянии, называются стандартными величинами. Изменения термодинамических величин при реакции, в ходе которой исходные вещества в стандартном состоянии превращаются в продукты реакции, ; также находящиеся в стандартном состоянии, называются ста н д артными изменениями соответствующих величин. [3]
Термодинамические величины, характеризующие вещество в его стандартном состоянии, называются стандартными величинами. Изменения термодинамических величин при реакции, в ходе которой исходные вещества в стандартном состоянии превращаются в продукты реакции, также находящиеся в стандартном состоянии, называются стандартными изменениями соответствующих величин. [4]
Термодинамические величины подразделяются на два типа: интенсивные и экстенсивные; такие свойства, как температура, плотность и давление, которые имеют одинаковые значения в любой точке гомогенной фазы, называются интенсивными, а такие, как объем, разного рода энергии и энтропия, которые пропорциональны количеству вещества в фазе, называются экстенсивными. Экстенсивная величина может быть преобразована в интенсивную путем деления ее на количество вещества, имеющегося в фазе. [5]
Термодинамические величины также очень важны в связи со свойствами фторуглеродных производных. Энергия связи С-F ( 115 ккал / моль-1) 7 больше, чем энергия связи С - Н ( 98 8 ккал / моль-1), поэтому устойчивость и реакционная способность углеводородных и фторуглеродных группировок значительно различаются. Многие исследователи8 указывали, что атомы фтора, более крупные по размеру по сравнению с атомами водорода, в противоположность углеводородам создают гораздо большую защиту углеродного скелета во фтор-углеродах. Поскольку для фторуглеродов требуются гораздо более высокие энергии активации, эта защита препятствует атакам реагентов на атомы углерода и значительно ограничивает выбор возможного механизма реакции. Следовательно, фтор-углеродная группа является, как правило, гораздо более стабильной единицей, чем соответствующая-углеводородная группа. [6]
Термодинамические величины очень важны для оценки возможных направлений разложения углеводородов и фторуглеродов. Например, пиролиз углеводородов приводит к потере водорода и образованию ненасыщенных углеводородов или угля. С другой стороны, оторвать фтор от фторуглерода с образованием олефина энергетически гораздо труднее. Действительно, энергия, необходимая для отрыва фтора, значительно выше энергии связи углерод - углерод, так что энергетически более выгодно расщепление молекулы, чем отрыв фтора. Разложение углеводородных и фторуглеродных производных, например три-метиларсина и трис ( трифторметил) арсина9, на начальной стадии, очевидно, одинаково, так как в обоих случаях образуются радикалы. Более того, энергии активации образования метального и трифторметильного радикалов очень близки, так же как, например, их поведение с ненасыщенными системами. Однако механизмы разложения этих радикалов совершенно различны. [7]
Термодинамические величины были рассчитаны для 298 16 К, путем экстраполяции уравнения температурной зависимости для константы равновесия ниже температурных пределов измерений. [8]
Термодинамические величины, характеризующие вещество в его стандартном состоянии, называются стандартными величинами. Изменения термодинамических величин при реакции, в ходе которой исходные вещества в стандартном состоянии превращаются в продукты реакции, также находящиеся в стандартном состоянии, называются стандартными изменениями соответствующих величин. [9]
Термодинамические величины бывают двух сортов. Одни из них ( экстенсивные) пропорциональны объему или массе системы. К ним относятся все потенциалы и, например, энтропия. Иногда в качестве параметров состояния удобно вводить число частиц в системе. Ей соответствует интенсивная переменная - химический потенциал ( см. гл. Если тело находится под воздействием внешних полей ( электрического и / или магнитного), то поля - интенсивные параметры, а поляризуемости ( электрическая и / или магнитная) - экстенсивные. [10]
Термодинамические величины, зависящие только от. Следовательно, 66-щая энергия Е представляет собой одну из таких функций. Зная, что Е является термодинамической функцией, мы можем написать ряд выражений, которые также будут описывать термодинамические функции. [11]
Термодинамические величины и уравнения классической термодинамики установлены для тел в собственной системе отсчета, в которой они покоятся. [12]
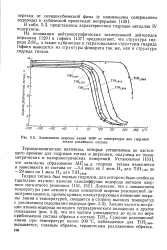 |
Зависимость ширины линий ЯМР от температуры для гидридов титана различного состава. [13] |
Термодинамические величины, которые установлены до настоящего времени для гидридов титана и циркония, получены из тензи-метрических и калориметрических измерений. [14]
Термодинамические величины для реакций рассчитывают как изменения в соответствующих свойствах компонентов реакции, считая, что происходит полное превращение исходных веществ в конечные. [15]
Страницы: 1 2 3 4