Вычисленная величина - энергия
Cтраница 1
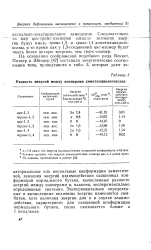 |
Разность энергий между изомерами диметилциклогексана. [1] |
Экспериментально определенные и вычисленные величины энергии изменяются сим-батно, хотя величина энергии для х в случае взаимодействия, характерного для скошенной конформации нормального бутана, снова оказывается ближе к 1 ккал / моль. [2]
Эти вычисленные величины энергий диссоциации связей еще не были проверены непосредственным измерением. [3]
В соответствий с вычисленной величиной энергии связей по Паулингу [8], реакция в газообразной фазе должна быть экэотермичной и протекать с выделением 5 7 кал. [4]
По данным тех же авторов вычисленная величина энергии активации сильно зависит от начального давления углеводорода. При низких давлениях указанные величины энергии активации сильно отлича - лись друг от друга. При экстраполяции же к бесконечному давлению все три кривые совпали практически в одной точке. Поэтому величину энергии активации необходимо вычислять с помощью констант скорости крекинга, экстраполированных к бесконечному давлению или найденных экспериментально при высоком давлении. [5]
Сопоставление эмпирических значений ПИт с вычисленными величинами энергии орбиталей является основным приемом для интерпретацииФЭ - спектррв. Не менее ценна и эмпирическая интерпретация, основанная на определенной характеристичности полос в спектре. Выбивание электронов из неподеленных электронных пар азота [10. 37] и фосфора [38] дает широкие полосы, разность между ПИ и ПИ в этом случае составляет около 0 5 эв, что связано как с участием неподеленных электронных пар этих атомов в связывании, так и с изменением геометрии иона при ионизации. [6]
 |
Мутаротация глюкозы в водном растворе при 18. [7] |
Однако в других случаях имеется несколько худшее совпадение наблюдаемых и вычисленных величин энергий активации и констант скорости. Так, например, мутаротация глюкозы в воде катализируется многими ионами и молекулами. Если применить определенный метод расчета, описанный в гл. [8]
Теоретические расчеты [7], основанные на применении циклов Борна - Габера и вычисленных величин энергии решеток, привели к выводу, что энергия диссоциации A1F на атомы равна 148 ккал, а теплоты образования твердого и газообразного A1F соответственно равны 103 и 50 ккал, что значительно больше теплот образования других моногалогенидов алюминия. [9]
Однако приведенный выше расчет слишком упрощен и в пего необходимо внести поправки; все поправки приводят к увеличению вычисленной величины энергии напряжения, а поэтому она значительно превосходит величину, полученную экспериментальным путем. Прежде всего два атома водорода в заслоненном положении у соседних атомов углерода [17,18] могут привести к увеличению энергии системы ( см. гл. Еслибыциклобутан был жестким квадратом, то все атомы водорода были бы в заслоненном положении и энергия соединения, возможно, увеличилась бы на 7 - 8 ккал / молъ. [10]
На кривой Ек ( рис. 5 - 10) виден небольшой минимум, что указывает на устойчивость молекулы, но вычисленная величина энергии составляет всего около 0 1 экспериментального значения. Если разобрать отдельные члены выражения для энергии, можно сделать вывод, что Ек по существу является энергией классического кулоновского взаимодействия между двумя атомами водорода. [11]
В результате было установлено, что при предположении об адсорбции дегидратированных катионов добавки получается правильное соответствие больших величин адсорбции более отрицательным потенциалам. Вычисленные величины энергии адсорбции имеют в этом случае порядок 1 - КГ12 эрг / ион. [12]
Это говорит о том, что процессом, контролурующим динамическое деформационное старение углеродистых сталей при статическом и динамическом растяжении, является диффузия атомов углерода и азота к дислокациям и связанная с этим блокировка дислокаций. Некоторое отличие вычисленной величины энергии активации от действительной величины энергии активации диффузии углерода и азота в железе объясняется, по-видимому, недостаточной точностью определения температур минимумов относительного удлинения и сужения на графиках температурной зависимости при динамическом разрыве из-за слишком большой растянутости минимумов по температурной шкале, а также тем, что при таком определении энергии активации не учитывается влияние скорости деформации на плотность дислокаций и характер их распределения. [13]
Однако общий метод сведения к минимуму энергии ( по отношению ко всем возможным расположениям молекулы) представляется очень действенным. Только там, где достигнут минимум энергии как в отношении деформации связи, так и в отношении вандерваальсового взаимодействия, вычисленная величина энергии активации приближается к экспериментально найденной величине. [14]
Если на кривой потенциальной энергии имеется минимум, значит теория предсказывает существование устойчивой молекулы. На рис. 5 - 10 вторая кривая изображает Ек, на ней виден небольшой минимум, что указывает на устойчивость молекулы, но вычисленная величина энергии составляет всего около 0 1 от экспериментального значения. [15]
Страницы: 1 2