Распад - метан
Cтраница 3
До выполнения основных экспериментов были проведены опыты по определению каталитической активности меди к реакции распада метана, так как в литературе не было данных по этому вопросу. Эти опыты показали, что в интервале температур 800 - 850 медь не оказывает заметного каталитического действия на эту реакцию. Степень разложения метана в указанном интервале-температур на поверхности меди и на поверхности кварца была, примерно одинаковая. [31]
Для развития радикально-цепного распада через промежуточное образование метил-радикалов кинетический расчет приводит к полуторному порядку валовой реакции распада метана. [32]
Таким образом, этими обстоятельными исследованиями было установлено, что механизм начальной стадии крекинга метана включает в качестве первичной реакции распад метана на СНз и атом Н, происходящий на поверхности, а вторичной реакцией, катализирующей распад метана, является гетерогенный распад метил-радикалов, при котором появляются метиленовые радикалы. Последние, взаимодействуя с метаном на поверхности, могут доставлять этилен, а в юбъеме - метил-радикалы. [33]
Рейс и др. установили с несомненностью, что в результате действия высокой температуры из углеводородов образуются радикалы и в частности при распаде метана можно ожидать образования свободных радикалов ОН, СНз, - СНэ и других, соответственных им, если исходные углеводороды были не СШ, а более высокомолекулярные. Из этих осколков и может синтезироваться бензол, его гомологи или би -, три - и полициклические соединения. [34]
Пакет, а затем Рейс и др. установили с несомненностью, что при действии высокой температуры из углеводородов образуются радикалы и в частности при распаде метана можно ожидать образования свободных радикалов СН, СН2, - СНз и других, соответственных им, если исходные углеводороды были не CHj, а более высокомолекулярные. Из этих осколков и может синтезироваться бензол, его гомологи или би -, три - и полициклические соединения. [35]
Так как связь С - С в образующемся этане на 71 кДж / моль ( 17 ккал / моль) слабее связи СН3 - Н, распад метана идет с самоускорением в результате увеличения скорости инициирования цепей при накоплении этана. Рассмотрим влияние температуры и давления на результаты термического разложения парафиновых угле водородов. [36]
Вместе с опытами по непосредственному обнаружению метиленовых радикалов в зоне распада метана [173] приведенный выше анализ кинетических зависимостей, казалось, свидетельствует о большей вероятности механизма распада метана через метиленовые радикалы. Этот механизм казался более вероятным и в случае распада этана, поскольку, подобно СО, образование метилен-радикалов как более стабильных частиц может пройти энергетически более экономно. [37]
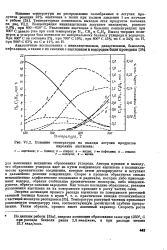 |
Влияние температуры на выходы летучих продуктов пиролиза ацетилена. [38] |
По данный работы [ 35а ], энергия активации образования сажи при 1250 С при распаде бензола равна 2 8 ккал / моль, а при распаде метана 32 7 ккал / моль. [39]
Таким образом, последние две реакик идут-ие на поверхности, а в объеме, и поэтому вполне возможно, поды екав сильно действующий каталитический яд, затормозить элемеь тарный распад метана. [40]
Данные для равнове: ия предыдущей реакции не могуг применяться для температур ниже 700 - 830 С, так как реакция ( 1) в этих условиях не течет, а наблюдается процесс распада метана до аморфного углерода. Свойства аморфного углерода, а также и его свободная энергия сильно зависят от условий его выделения. [41]
Таким образом, этими обстоятельными исследованиями было установлено, что механизм начальной стадии крекинга метана включает в качестве первичной реакции распад метана на СНз и атом Н, происходящий на поверхности, а вторичной реакцией, катализирующей распад метана, является гетерогенный распад метил-радикалов, при котором появляются метиленовые радикалы. Последние, взаимодействуя с метаном на поверхности, могут доставлять этилен, а в юбъеме - метил-радикалы. [42]
Недостаточное совпадение уравнения ( 4 - 20) с опытными данными Введенский и Фрост объясняют тем, что свободная энергия углерода, выделяющегося при распаде СН4, отнюдь не равна свободной энергии графита, что бесспорно справедливо для низких температур распада метана. Между тем уравнение ( 3 - 20) прилежимо к графиту. [43]
Его термическая деструкция термодинамически возможна при температуре выше 560 С. С заметной скоростью распад метана протекает при температуре выше 1000 С. При высокотемпературном пиролизе метана, кроме водорода ( и пиро - ), образуются этилен, этан, ацетилен и арены. [44]
Термический распад метана [ реакция (8.14) с выделением сажи на Ni ] протекает до / 350 С. При повышении температуры распад метана замедляется из-за отложений сажи на поверхности никеля. [45]
Страницы: 1 2 3 4